Concentrație mare de siliciu. Știi cum
Procesor? Pisok? Și ce ai cu asocierile de cuvinte? Sau poate Silicon Valley?
De parcă n-ar fi fost acolo, cu siliciu lipim astăzi și dacă trebuie să știi ce este Si și de ce mănânci, cer o pisică.
Intrare
Fiind student la una dintre universitățile din Moscova la specialitatea „Nanomateriale”, vreau să te cunosc, dragă cititor, cu cele mai importante elemente chimice ale planetei noastre. Aleg ceva de mult timp, cărbune sau siliciu, și totuși am decis să folosesc Si eu însumi, astfel încât inima oricărui gadget modern să se bazeze pe el însuși, așa că poți spune atât de splendid. Voi încerca să îmi fac gândurile extrem de simple și accesibile, după ce am scris acest material, l-am salvat, în principal pentru începători, dar tot mai mulți oameni îl pot obține de la cicave, așa că aș dori să spun că articolul a fost scris. exclusiv pentru extinderea intereselor, ceea ce s-a blocat. Și deci să începem.
Siliciu
Siliciu (lat. Siliciu), Si, element chimic din grupa IV a sistemului periodic Mendeliev; numar atomic 14, greutate atomică 28.086.
În natură, elementul este reprezentat de trei izotopi stabili: 28Si (92,27%), 29Si (4,68%) și 30Si (3,05%).
Grosime (n.s.) 2,33 g/cm?
Punct de topire 1688 K

Pulbere Si
Dovada istorica
Dealuri de Siliciu, terenuri întinse, bulevarde de oameni din epoca de piatră. Erau mii de șproți de piatră și udarea pietrei. Zastosuvannya spoluk Siliciu, legat de prelucrarea lor, - pregătirea unui depozit - a început în jurul anului 3000 î.Hr. e. (Vechiul Egipt). Mai devreme, în casă, a fost folosit siliciu - oxid SiO2 (silice). În secolul al XVIII-lea, siliciul era injectat cu un corp simplu și transportat în „pământuri” (care este folosit în numele său). Skladnіst la un depozit de silice care a instalat І. I. Berzelius. În aceeași vpershe, în 1825, după ce a îndepărtat siliciul elementar din fluorura de siliciu SiF4, înlocuind restul de potasiu metalic. Noul element a fost numit „siliciu” (lat. silex - silex). Nume rusesc vvіv G. I. Hess la 1834 roci.

Arc de siliciu al extensiilor în natură la depozitul sunetului sonic
Siliciu în expansiune în natură
Pentru lățimea scoarței terestre, siliciul este un alt element (după acru), media sa în litosferă este de 29,5% (în spatele masei). Scoarța pământului, gri silicon, are același rol principal, ca și cărbunele din lumea pământească a creaturii. Pentru geochimia siliciului, este important, în special, că legătura dintre yogo și sour este importantă. Aproape 12% din litosferă devine silice SiO2 sub formă de cuarț mineral și diverse varietăți. 75% din litosferă este compusă din diverși silicați și aluminosilicați (polova, mica, amphibole toshcho). Numărul total de minerale, care pot fi înlocuite cu silice, depășește 400.
Puterea fizică a siliciului
Cred că mai ales nu este varto, asta-i tot Puterea fizică Am acces gratuit, dar le voi enumera pe cele mai comune.
Punct de fierbere 2600 ° C
Prozorium de siliciu pentru dovgokhvilovyh ІCh-promenіv
Pătrunderea dielectrică 11.7
Duritate Mohs Silicon 7.0
Aș dori să spun că materialul de siliciu tenditny, deformarea plastică comemorativă începe la temperaturi mai mari de 800°C.
Siliciul este un dirijor, același vin pe care îl cunoaștem o mulțime de zastosuvannya. Puterea electrică a siliciului poate sta în casă.
Putere chimică.
Este bogat aici, este uimitor, s-ar putea spune, dar mă poticnesc cu cel mai faimos. În rafturile de Si (similar carbonului) 4-valent.
Pe suprafața zavdyak-ului de siliciu, topirea oxidului este stabilă la vânt la temperaturi ridicate. În acid, se oxidează la 400 °C, dizolvând oxidul de siliciu (IV) SiO2.
Siliciu rezistent la acizi și este mai puțin probabil să fie amestecat cu acizii azotic și fluorhidric, ușor de distins în pajiștile fierbinți de apă observată.
Siliciul face 2 grupe de silani acizi - siloxan și siloxeniu. Siliciul reacţionează cu azotul la temperaturi peste 1000 °C. este un material valoros pentru industria chimică, precum și pentru producția de stingătoare. Duritatea ridicată, precum și rezistența termică și chimică, sunt tratate cu pardoseli cu carbură de siliciu (carbură de siliciu SiC) și bor (SiB3, SiB6, SiB12).
Otrimanya Silicon
Cred că tse naytsіkavіsha parte, aici este raportul.
Tipul de recunoaștere nedorit este împărțit:
1.
Putere electronică din silicon(t.z. siliciu electronic"") - cel mai silicios din ceața de siliciu peste 99,999% din spatele peretelui, suportul electric al calității electronice de siliciu poate fi schimbat în intervalul de aproximativ 0,001 până la 150 ohm cm, dar cu care valoarea suportului este de vina buti este prevazut cu o casa all-inclusive, astfel incat sa puteti intra in cristalul altora casa, dorind sa se ocupe de sarcinile pepiniera de opir electric, suna, inacceptabil.
2.
Siliciu de calitate Sony(t.z. "sonyachny silicon") - siliciu din siliciu amestecat peste 99,99% pe fibră, care este utilizat pentru producerea dispozitivelor de conversie fotoelectrice (baterii sonice).

3.
Siliciu tehnic- blocuri cu structură policristalină de siliciu, luate prin metoda reînnoirii carboterme din pur scârțâit de cuarț; acoperire cu 98% siliciu, casa principală este cărbune, este aerisită cu o cantitate mare de elemente ușoare - bor, fosfor, aluminiu; folosit în principal pentru deținerea siliciului policristalin.
Siliciul de puritate tehnică (95-98%) posedă explozii electrice de silice inspirată SiO2 între electrozii de grafit. La legătura cu dezvoltarea nap_v_dnikovoї tehnіko razrobleno metoda de obținere a siliciului pur și mai ales pur. De dragul sintezei înainte de siliciu pur vih_dnih spoluk, z yakikh vityagyat silіkі vіdnovlennya vіdnovlennya аbo termіchnogo razkladannya.
Siliciu policristalin ("polisiliciu") - cea mai pură formă de siliciu, care este viabilă din punct de vedere comercial, - un produs care este utilizat pentru purificarea siliciului tehnic prin metode cu clorură și fluorură și care este victorios pentru producerea de mono- și multi-cristalin. siliciu.
În mod tradițional, siliciul policristalin este îndepărtat din siliciul tehnic cu o cale de transfer de yoga în robinete de silan (monosilan, clorosilan, fluorosilan) cu un fund ofensiv de silani, care sunt decontate, purificarea rectificată a silanului transformat și recondiționarea silanului în silan metalic. .
Conductoarele de siliciu pur se obțin în două tipuri: policristalin(întărirea SiCl4 sau SiHCl3 cu zinc sau apă, dilatare termică a SiI4 și SiH4) și monocristalină(Topirea și „înfășurarea” în zonă fără creuzet a unui singur cristal din siliciu topit - metoda Czochralsky).

Aici puteți folosi metoda Czochralski pentru a vibra siliciul.
metoda Czochralski- metoda de vibrare a cristalelor cu un traseu de înfăşurare în sus pe deal în aer pe suprafaţa marii obligaţii de a se topi cu iniţierea stiuletului de cristalizare cu calea aducerii cristalului sămânţă (sau a unui număr mare de cristale). ) de o structură dată și orientare cristalografică atsії în contact cu o topitură de suprafață liberă.
Zastosuvannya Silicon
Siliciul aliat special este utilizat pe scară largă ca material pentru pregătirea conductorilor electrici (tranzistoare, termistoare, vibratoare de putere, tiristoare; fotocelule Sony care sunt utilizate în nave spațiale, precum și o mulțime de tot felul de lucruri).
Cioburi de prosorie de siliciu pentru schimbarea de la firele lungi de par in dimensiunea de la 1 la 9 microni, pot fi plasate in optica infrarosu.
Siliciul poate fi diferit și toate zonele zastosuvannya, care se extind. In metalurgie Si
vikoristovuetsya pentru îndepărtarea acrișiunii (dezoxidării) din metalele topite.
Siliciu depozit un număr mare de aliaje ale halei și metale de culoare.
Aliaje de siliciu sunet pentru creșterea rezistenței la coroziune, îmbunătățirea puterii lor livar și creșterea rezistenței mecanice; prote cu o mai mare zmistі Siliciul poate viklikati kryhkіst.
Cele mai importante sunt aliajele, cuprul și aliajele de aluminiu, care pot fi folosite pentru a răzbuna curelele.
Siliciul este prelucrat prin sticlă, ciment, ceramică, electrice și alte galize industriale.
Curățarea siliciului este importantă pentru fabricarea de dispozitive electronice individuale (de exemplu, procesorul computerului dvs.) și microcircuite cu un singur cip.
Siliciul pur, folosit pentru siliciul pur, purificarea siliciului metalurgic ca siliciu cristalin este principala materie primă pentru energia Sony.
Siliciu monocristal - crema electronică și ingineria energetică Sony este folosită pentru realizarea oglinzilor laserelor cu gaz.

Siliciu de curățare și un produs de yoga
Siliciu în corp
Siliciul din corp se găsește în ochii diverșilor spoluk, care participă la rangul principal în iluminarea părților și țesuturilor dure ale scheletului. Deosebit de bogat în siliciu, se pot acumula deaks de alge marine (de exemplu, alge diatomee) și creaturi (de exemplu, bureți din corn de siliciu, radiolarie), care la momentul oceanului pe fundul oceanului sunt întărite de depozite de oxid de siliciu. (IV). În mările și lacuri reci, catârii biogene, bogati în siliciu, sunt mai importanți, în mările tropicale - catâri de vapoare cu conținut scăzut de siliciu. Ierburi, rogoz, palmieri și coada-calului acumulează mult siliciu în mijlocul creșterilor terestre. În coloana vertebrală creaturile, în loc de oxid de siliciu (IV), în râurile de cenușă 0,1-0,5%. În cel mai mare număr de manifestări de siliciu în alcalin țesătură fericită, nirkah, bolta pidshunkovy. Într-o dietă suplimentară, oamenii au până la 1 g de siliciu. Cu un aport mare de oxid de siliciu (IV) în aer, acesta este consumat în legenia unei persoane care provoacă boală - silicoza.
Visnovok
Ei bine, din toate, dacă ai citit până la capăt și ai pătruns puțin, atunci ești puțin mai aproape de succes. M-am spodіvayus, scriind nu degeaba și pіst vouchsafed to hoch komu. Pentru respect.
SILICIU. (Siliciu), Si - chimic. elementul IV al grupului sistemului periodic de elemente; la. n. 14, la. m. 28.086. Siliciu cristalin - vorbire gri închis, cu o strălucire rășinoasă. În cele mai multe cazuri, se dezvăluie gradul de oxidare - 4, +2 și +4. Siliciul natural este alcătuit din izotopi stabili 28Si (92,28%), 29Si (4,67%) și 30Si (3,05%). Retragerea izotopilor radioactivi 27Si, 31Si și 32Si cu perioade de dezintegrare inversă de 4,5 secunde, 2,62 ani și 700 de ani. văzut pentru prima dată în 1811 în franceză. chimistul şi fizicianul J. L. Gay-Lussac şi French. chimistul L. J. Tenar, dar există mai puține identificări în 1823 suedez, chimist și mineralog J. Ya. Berzelius.
Pentru lățimea scoarței terestre (27,6%), siliciu-alt element (după acru). Cunoașterea este importantă. sub forma de silice Si02 si alte vorbiri acre (silicati, aluminosilicati etc.). Pentru cei mai buni minți, se stabilește o modificare stabilă a șervețelului, care are o structură cubică centrată pe față precum diamantul, cu o perioadă de a = 5,4307 A. Pătrunderea intermitentă este de 2,35 A. Lățimea este de 2,328 gcm. Cu o presiune mare (120-150 kbar) treceți la fire mai mari și modificări metalice. Modificarea metalului-superconductor cu o temperatură de tranziție de 6,7 K. Odată cu creșterea presiunii, punctul de topire scade de la 1415 ± 3 ° C la o presiune de 1 bar la 810 ° C la o presiune de 15.104 bar rar). ). Când este topit, există o creștere a numărului de coordonare și metalizarea legăturilor interatomice. Caracter silicic amorf de ordinul scurt, care prezintă o structură cubică puternic creată centrată pe volum, aproape de rară. Debievskaya t-ra este aproape de 645 K. Coef. expansiunea liniară a temperaturii se modifică cu modificarea t-ri conform legii extreme, mai mică decât t-ri 100 La vin devine negativă, atingând minimul (-0,77 10 -6) deg -1 la t-ri 80 K; la t-rі 310 K vinul este 2,33 10-6 deg-1, iar la t-rі 1273 K-4,8 10 deg-1. Căldura de fuziune 11,9 kcal/g-atom; tkіp.3520 K.
Căldura de sublimare și evaporare la temperatura de topire este de 110 și 98,1 kcal/g-atom. Conductivitatea termică și conductibilitatea electrică a siliciului se află în puritatea și minuțiozitatea cristalelor. Zі rostannyam t-ri coef. conductivitatea termică a K. pur crește treptat (până la 8,4 cal/cm X X sec deg la t-ri 35 K), apoi se modifică, ajungând la 0,36 și 0,06 cal/cm sec deg la t-ri vіdpovidno 300 și 1200 K. Entalpia, entropia și capacitatea de căldură K. în mințile standard, este egală cu 770 cal/g-atom, 4,51 și 4,83 cal/g-atom - deg. Siliciu diamagnetic, susceptibilitate magnetică a solidului (-1,1 10 -7 mu/g) și rar (-0,8 10 -7 mu/g). Siliciul este slab depus în t-ri. Energia de suprafață, grosimea și vâscozitatea cinematică de rare K. la temperatura de topire devin 737 erg/cm2, 2,55 g/cm3 și 3 10 m2/sec. Un conductor tipic de siliciu cristalin cu o lățime a zonei îngrădite de 1,15 ev la t-p 0 până la 1,08 u - la t-p 300 K. La temperatura camerei, concentrația sarcinilor care transportă umezeala este aproape de 1,4 10 10 cm - 3;
Puterea siliciului de a cădea datorită naturii și concentrării caselor, precum și perfecțiunii cristalului. Inel pentru otrimannya napіvprovіdnikovogo Do. cu conducerea yoga de tip r și n, ele sunt combinate cu elementele IIIb (bor, aluminiu, galiu) și subgrupul Vb (fosfor, mish'yak, antimoniu, bismut), care creează sukupnіst vіdpovіdno pentru acceptor și donator rіvnі în , roztashovannyh lângă cordoanele de zone. Pentru alierea vicoristului, acele alte elemente (de exemplu) sunt astfel modelate. glybokі rivnі, yakі obumovlyuyut îngropare și recombinare a taxelor noesіїv. Tse vă permite să luați materiale cu electro mare. susține (1010 ohm cm la t-rі 80 K) acea mică trivalitate a bazei sarcinilor minore de uzură, care este importantă pentru creșterea numărului de anexe diferite. Coeficient puterea termoelectrică cu siliciu trebuie doar depusă în t-ri și în locul casei, zbіlshyuyuchi zі zrostannym elektroopor (la p = 0,6 ohmi - cm, a = 103 microvolți / grindină). Pătrunderea dielectrică a siliciului (de la 11 la 15) este slab depusă în depozit și rigurozitatea monocristalelor. Legile argilării optice a siliciului sunt modificate foarte mult din cauza schimbării purității, concentrației și naturii defectelor în viață, precum și longevității.
Cordonul de lut indirect al kolivanului electromagnetic este aproape de 1,09 euro, lut direct - până la 3,3 euro. În regiunea vizibilă a spectrului parametrilor indicatorului complex de fractură (n - ik), este deja posibil să se întindă pe suprafața casei. Pentru Do deosebit de pur. (laλ \u003d 5461 A și t-re 293 K) n \u003d 4,056 și k \u003d 0,028. Producția electronică a robotului este aproape de 48 de euro. Tendință silicon. Duritate Yogo (t-ra 300 K) pentru Moos - 7; HB = 240; HV y \u003d 103; I = 1250 kgf/mm2; modulul de norme, elasticitate (policristal) 10890 kgf/mm2. Între mineralitate să se culce în adâncimea cristalului: pe vigin, adâncimea este de la 7 la 14; coef. Rigiditate 0,325 1066 cm2/kg.
La temperatura camerei, siliciul practic nu interacționează cu reactivii de tip gaz (inclusiv) și solizi, krіm lіv. La deplasarea t-ri, există o interacțiune activă cu metale și nemetale. Zocrema, care dizolvă carbura de SiC (la temperatură 1600 K), nitrură de Si3N4 (la temperatură 1300 K), fosfură SiP (la temperatură 1200 K) și arseniura Si As, SiAS2 (la temperatură 1000 K). Cu reacție acru la o temperatură de 700 K, stingerea dioxidului de Si02, cu halogeni - fluorură de SiF4 (la o temperatură mai mare de 300 K), clorură de SiCl4 (la o temperatură de peste 500 K), bromură de SiBr4 (la o temperatură de 700 K) i nodură SiI4 (la p.t. 1000). Reacționează intens cu mulți alții. metale, stabilind diferențe solide în înlocuirea lor cu chi chem. pe jumătate - siliciuri. Zonele de concentrare de omogenitate a trandafirilor solizi apar în funcție de natura rozetei (de exemplu, Nimechchin în 0 până la 100%, toamna până la 15%, în alfa zirconiu mai puțin de 0,1%).
Diferența dintre metale și nemetale în siliciul solid este semnificativ mai mică și sună retrograd. Cu ce granițe, în loc de casă, ce se face la Do. nu foarte adânc, atingeți maximul ( 2 10 18 , 10 19 , 2 10 19 , 1021, 2 10 21 cm) zona t-r vіd 1400 la 1600 K. Case cu rіvenny adânc vіdznyayutsya rozchinnіstyu ușor mai mic (vіd 1015 pentru seleniu și 5 10 16 pentru zalіza până la 7 10 17 pentru nichel și 10 18 cm pentru midi). La un oțel rar, siliciul nu este înconjurat de metale obișnuite, adesea cu mari viziuni de căldură. Siliciul pur este preparat dintr-un produs tehnic 99% Si і - 0,03% Fe, Al і Co), temperat cu cuarț și cărbune în cuptoare electrice. Începeți cu o nouă suflare până acolo (sum_shy clorhidric și sirchanoy, apoi fluorură-apă și sirchanoy) case, după care produsul (99,98%) este luat, tratat cu clor. Sintezele sunt purificate prin distilare.
Conductorul de siliciu este utilizat în combinație cu clorura de SiCl4 (sau SiHCl3) în apă sau expansiunea termică a hidrurii de SiH4. Purificarea reziduală și măcinarea monocristalelor se efectuează cu o metodă netedă a zonei fără creuzet sau prin metoda Czochralsky, ținând cont în special de sosul pur (în casă până la 1010-1013 cm-3) cf\u003e 10 3 ohm cm. iv la pe care să se introducă dozarea numărului de case necesare. Asa prepari creme cilindrice cu diametrul de 2-4 si lungimea de 3-10 cm.Pentru special. scopul este de a produce și mai multe monocristale. Siliciu tehnic și în special aliaje yogo din soluție salină vicorosă, cum ar fi oțeluri și aliaje acide, precum și aditivi ușori. K. monocristal zrazki deosebit de pur, dopat cu diferite elemente, este cunoscut ca bază a diferitelor atașamente cu curent scăzut (zocrema, termoelectrice, radio, lumină și fototehnice) și cu curent ridicat (vibrații, conversii).
Siliciu și siliciu
Siliciul este adus la nemetale, iar 4 electroni pot fi la același nivel de energie. Vіn poate vіddavati їх, arătând stadiul de oxidare + 4 și adăugați electroni, arătând stadiul de oxidare - 4. Cu toate acestea, capacitatea de a adăuga electroni la siliciu este semnificativ mai mică, mai mică decât carbonul. Atomii de siliciu pot avea o rază mai mare, atomi de carbon mai mici.
Cunoștințele naturii despre siliciu .
Arc de siliciu al extensiilor în natură. pe її parte din cădere pon peste 26% din masă rujeola pământului. Pentru lățimea vinurilor, stați în alt loc (după acru). Pe vіdmіnu vіd vіd uglec C vіlny stіnі vіrіdі nu zustrichaetsya. Intră în depozitul diferitelor compoziții chimice, în principal diverse modificări ale oxidului de siliciu (IV) și sărurilor acizilor silicici (silicați).
Obsesia pentru siliciu .
Siliciul de calitate industrială de puritate tehnică (95 - 98%) este dominat de SiO 2 cocs în cuptoarele electrice în timpul prăjirii:
SiO 2 + 2C \u003d Si + 2CO
SiO 2 + 2Mg \u003d Si + 2MgO
În acest fel, din case se ia pulbere de siliciu amorf de culoare maro. Recristalizarea din topirea metalelor (Zn, Al) poate fi transferată într-o moară de cristal.
Tetraclorura de siliciu, chiar și de înaltă puritate, este utilizată la 1000°C pentru tetraclorura de siliciu SiCl 4 perechi de zinc:
SiCl 4 + 2Zn \u003d Si + 2ZnCl 2
acel yogo de curățare urmând metode speciale.
Fizic Putere chimică siliciu.
Siliciu cristalin pur - pantă tendință și tare, flăcătoare. Ca un diamant, are o rețea cristalină cubică cu o legătură de tip covalent. Punct de topire Yogo 1423 °C. Pentru cele mai mari minți, un element inactiv de siliciu, care reacționează doar cu fluorul, dar când este încălzit, intră în diferite reacții chimice.
Yogo vikoristovuyut ca material valoros pentru napіvprovіdnikovіy tehnіtsі. Împreună cu alți conductori de vin, se distinge printr-o rezistență semnificativă împotriva acizilor diluați și o mare rezistență electrică până la 300 ° C. Siliciu tehnic și ferosiliciu vicorist și în metalurgie pentru oțeluri rezistente la căldură, rezistente la acizi și pentru scule, chavuns și alte aliaje bogate.
Cu metale siliconice chimii, Numiți siliciuri, când este încălzit cu magneziu, siliciura de magneziu se dizolvă:
Si + 2Mg = Mg2Si
Siliciurile metalelor din spatele structurii acestei dominante prezic carburi, astfel încât siliciurile asemănătoare metalelor, la fel ca carburile asemănătoare metalelor, se disting prin duritate mare, punct de topire ridicat, conductivitate electrică la cald.
Când prăjiți sumish pisku cu cocs în cuptoare electrice, carbura de siliciu și carbonul sunt amestecate cu carbură de siliciu sau carborundum:
SiO2 + 3C = SiC + 2CO
Carborundum este un discurs dur refractar, fără bare, un material abraziv și călduros valoros. Carborundum, iac i, grati cristalin maє atomic. La stația curată există un izolator, dar în prezența casei devine conductor.
Iac de silicon i , dizolvă doi oxizi: oxid de siliciu (II) SiO și oxid de siliciu (IV) SiO 2 . Oxidul de siliciu (IV) este un discurs dur refractar, larg lărgit în natură în țara liberă. Vorbirea stabilă din punct de vedere chimic, care interacționează numai cu fluorul și fluorul asemănător gazului din apă sau acid fluorhidric:
SiO 2 + 2F 2 \u003d SiF 4 + O 2
SiO 2 + 4HF \u003d SiF 4 + 2H 2 O
Arătarea directă a reacțiilor se explică prin faptul că siliciul poate avea o mare sporiditate față de fluor. În plus, tetrafluorura de siliciu este un discurs zburător.
La tekhnіtsі prozoriya SiO 2 vykorovuyut pentru prepararea unei plăci de cuarț refractar stabil, ca o dor de schimbarea ultraviolete, poate avea un coeficient mare de dilatare, care arată schimbări semnificative de temperatură. Modificarea amorfă a oxidului de siliciu (II) tripoli are o mare porozitate. Yogo vikoristovuyut ca izolator de căldură și sunet pentru vibrarea dinamitei (nasul vibukhovo discurs) și așa mai departe. Oxidul de siliciu (IV) într-un sunet vibrant este unul dintre principalele materiale de zi cu zi. Este vicoros în producția de materiale rezistente la foc și acizi, oțel, ca un flux în metalurgie și așa mai departe.
Conform formulelor moleculare, puterea chimică și fizică a oxidului de carbon (IV) și a oxidului de siliciu (IV) este ușor de egalat, puterea acestora este similară în depozit chimic z'ednan raznі. De ce se explică faptul că oxidul de siliciu (IV) se formează nu doar din molecule de SiO 2 , precum s їх asociați, în unele dintre ele atomii de siliciu sunt uniți între ei prin atomii de acru. Oxid de siliciu (IV) (SiO 2 )n. Imaginea її pe pătrat:
Un alt reprezentant al elementelor subgrupului principal al grupei IV (grupa IVA) a sistemului periodic al lui D. I. Mendeliev - siliciu Si.
În natură, siliciul este un alt element chimic pentru lățimea acidului. Scoarța terestră este din ce în ce mai pliată trimestrial din yogo spoluk. Cel mai răspândit siliciu este oxidul de siliciu (IV) SiO 2, celălalt nume este silice. În natură, vinurile sunt făcute cu cuarț mineral (mic 158), o varietate bogată de astfel de - cristal girsky, și, de asemenea, faimoasa formă de liliac - ametist, precum și agat, opal, jasp, calcedonie, carnelian, sub formă de virobnі și pietre îmbătătoare. Oxidul de siliciu (IV) este, de asemenea, compus dintr-un nisip remarcabil și cuarțos.

Mal. 158.
Cristale de cuarț intercalate în dolomit
Trei minerale diferite pe bază de oxid de siliciu (IV) (slex, calcedonie și altele) primii oameni pregătit znaraddya pracі. Același silex, care este discret și nu mai îngust decât o piatră, așezând stiulețul unei pietre vіtsі - vіtsі kremіnyh znaryad pratsі (Fig. 159). Există două motive pentru aceasta: lățimea și disponibilitatea silexului, precum și construcția de clădiri cu cât de ascuțite sunt marginile.

Mal. 159.
Znaryaddya piatra vіku
Un alt tip de materiale naturale pentru siliciu este silicatul. Printre acestea se numără cele mai mari lățimi de aluminosilicați (s-a înțeles că acești silicați pot înlocui elementul chimic de aluminiu). Granitul se adaugă la aluminosilicați, vezi diferit argila, mica. Silicatul, care nu răzbună aluminiul, de exemplu, azbestul, care este folosit la fabricarea artificiilor.
Oxidul de siliciu (IV) SiO 2 este necesar pentru viața cultivatorilor și a creaturilor. Vinurile dau tulpini de roslin și zahisnymi voaluri de creaturi (Fig. 160). Cozile de zavdyaki yomu, cozile și coada-calului stau mitzno, ca niște pungi, rozii cu frunze de gostre tăiate, precum cuțite, miriște pe un câmp înclinat, ca un cap și tulpini de cereale pe podeaua unei mitzne, care nu permit câmpuri de porumb în câmp a se întinde într-o scândură şi vânt . Coasta Luska, scoici de comă, krill meteliks, pir'ya ptahiv în lână de creaturi de mіtsnі, oskіlki smite silica.

Mal. 160.
Oxidul de siliciu (IV) dă mineralitate tulpinilor de roslin și curbelor sufocante ale creaturilor
Siliciul Z'ednannya oferă netezime și catifelare părului și unghiilor unei persoane.
Siliciu pentru a intra și în depozitul organismelor vii inferioare - diatomee și radiolari, cei mai de jos sâni ai materiei vii, creându-și parcă imperfecțiunile în spatele frumuseții scheletului cu silice (Fig. 161).
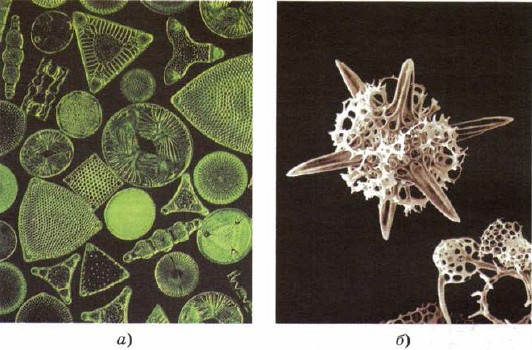
Mal. 161.
Scheletele de diatomee (a) și radiolarie (b) sunt compuse din silice
Dominația siliciului. Utilizați un microcalculator cu o baterie Sony și, prin urmare, există o notificare despre siliciul cristalin. Tse napіvprovіdnik. Pe vіdmіnu vіd metalіv, іz pіdvishennyam temperatura yogo elektroprovіdnіst zbіshuєtsya. Pe sateliți, nave spațiale, stații și dahah budinkiv (mici 162) instalează baterii Sony care convertesc energia Sony în electricitate. Duhoarea lucrează cristale de napіvprovіdnikіv și la primul silex negru. Fotocelulele din siliciu pot fi convertite în energie electrică până la 10% din energia Sony cu argilă.

Mal. 162.
Baterie somnoroasă pentru cabina dahu
Siliciu pentru a arde la aciditate, satisfacându-te cu oxid de siliciu (IV):
![]()
Fiind nemetal, atunci când este încălzit, siliciul se îmbină cu metalele cu soluții de siliciu, de exemplu:
![]()
Siliciurile sunt ușor de răspândit cu apă sau acizi, când vedeți un siliciu asemănător cu apa - silan:
Pe suprafața carbohidraților, silanul de pe suprafață se auto-angrenează și arde cu oxid de siliciu dizolvat (IV) și apă:
Reacția crescută între silan și metan CH 4 se explică prin faptul că expansiunea atomului de siliciu este mai mare, mai mică la carbon, deci legăturile chimice Si-H sunt mai mici, legăturile C-H sunt mai mici.
Interacțiunea siliciului cu schimbările concentrate ale apei din pajiști, producând silicat și apă:
Siliciul posedă, similar cu oxidul de siliciu (IV), magneziu sau carbon:
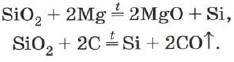
Oxid de siliciu (IV), sau dioxid de siliciu sau silice SiO 2 yak і CO 2 є oxid acid. Cu toate acestea, pe suprafața CO2 există o rețea cristalină moleculară, dar atomică. Pentru că SiO 2 este vorbire dură și refractară. Vinurile nu diferă în acizi de apă, acid fluorhidric, aloe la temperaturi ridicate cu pajiști cu săruri dizolvate de acid silicic - silicați:
Siliciul poate fi folosit și pentru a alia oxidul de siliciu (IV) cu oxizi sau carbonați metalici:
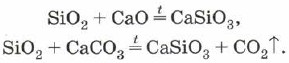
Silicații de sodiu și potasiu sunt numiți plăci de vânzare cu amănuntul. Їх rezerva de apa- Este bine să folosiți clei de silicat.
Acid silic H 2 SiO 3 (Fig. 163):
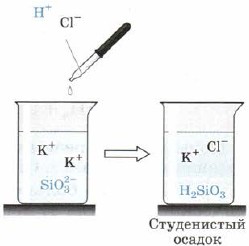
Mal. 163. Reacția acidă la ion silicat
De asemenea, H2SiO3 este, de asemenea, un acid slab. Este inconsecvent în apă și cade din frământarea reacționară în privința drojdiei asediului, care uneori comprimă întregul volum al diferenței, transformându-l într-o masă solidă, merg la jeleu, jeleu. La agățarea mașii, se stabilește un discurs foarte poros - silicagel, care este utilizat pe scară largă ca adsorbant - argilă a altor discursuri.
Certificat de laborator nr 40
Posesia acidului silicic și acea justificare a puterii
Injecție de siliciu. Știți deja că siliciul este folosit pentru producerea materialelor conductoare, precum și a aliajelor rezistente la acizi. Când nisipul de cuarț este topit cu lână la temperaturi ridicate, carbura de siliciu SiC este dizolvată, care este disponibilă numai pentru diamant. Prin urmare, este necesar să vicorate pentru ascuțirea rіztsіv metalorіzalnyh verstatіv și lustruirea pietrei scumpe.
Din cuarț topit se prepară diverse vase chimice de cuarț, care pot rezista la temperaturi ridicate și nu se crăpă la rece.
Z'ednannya silicon є baza pentru deformarea depozitului la ciment.
Eroarea Zvichayne poate fi depozitată, care poate fi exprimată prin formula Na 2 O CaO 6SiO 2. Yogo este câștigat la cuptoare speciale de gătit cu sifon sumish, vapnyak și piska.
Vіdmіnna orez skla - zdatnіst rozm'yakshuvatisya în umflarea oțelului topit indiferent dacă este o formă, deoarece este salvat atunci când depozitul este prins. Pe baza carora se fac ustensilele si se fac celelalte marfa.
Dodatkovі yakosti sklu da diferiți aditivi. Deci, introducerea oxidului de plumb este redusă la o culoare cristalină, oxidul de crom devine verde, oxidul de cobalt este albastru etc. (Fig. 164).

Mal. 164.
Produse din depozitul de culori
Sklo este unul dintre cei mai vechi vinificatori ai poporului. Deja 3-4 tisa. Din acest motiv, războiul a izbucnit în Egipt, Siria, Finiki și Marea Neagră.
Sklo - același material nu este mai puțin decât remіsnikіv, dar și artiști. Stăpânul a atins cel mai înalt nivel de perfecțiune Roma antică, de parcă ar fi putut să îndepărteze panta de culoare și lucrul mozaicurilor lor.

Mal. 165.
Sticlă colorată la vitraliile Catedralei Notre Dame, Chartres
Creați opere de artă din depozit cu atributele obov'yazkovymi ale unui mare muzeu și vitralii colorate ale bisericii, panouri de mozaic - capturi luminoase ale acestui (Fig. 165). Într-una dintre incintele filialei din Sankt Petersburg a Academiei Ruse de Științe, există un portret în mozaic al lui Petru I, victorios M. V. Lomonosov (Fig. 166).

Mal. 166.
Portretul în mozaic al lui Petru I
Zonele de aglomerație sunt destul de mari. Tse vikonne, plyashkove, lampov, dzerkalne sklo; panta optică - de la oculare la ochelari de cameră; lentile de dispozitive optice care nu se pot distinge - de la microscoape la telescoape.
Al doilea material ca importanță, acoperirile pe bază de siliciu, este cimentul. Yogo este folosit pentru coacerea argilei și vaparea în cuptoare speciale care sunt ambalate.
Dacă pulberea de ciment este amestecată cu apă, atunci cimentul nu este ferm stabilit, altfel, așa cum se numește ceasuri cu alarmă, ciment rozchin, care este pas cu pas mai greu. Când adăugați beton în ciment sau piatră zdrobită, betonul trebuie îndepărtat ca un strat de acoperire. Materialitatea betonului este în creștere, astfel încât în cel nou se introduce un nou cadru - iese betonul turnat, din care se realizează pereții panoului, blocuri de suprapuneri, poduri fermi etc.
Depozitul este angajat în producția de ciment industria silicatilor. Vaughn produce și ceramică cu silicați - ceglu, porțelan (mic 167), faianță și articole din acestea.

Mal. 167.
Soiuri de porțelan
Vіdkrittya silicon. Chiar dacă în antichitate oamenii au câștigat pe scară largă în utilizarea siliciului, siliciul în sine a fost luat pentru prima dată în 1824 de chimistul suedez J. Ya. Berzelius. Cu toate acestea, cu 12 ani înainte de noul silex, J. Gay-Lussac și L. Tenard au fost luați, ale vin duzhe zabrudneniy case.
Numele latin silicum își ia stiulețul de la cuvântul latin silex-flint. Numele rusesc „silicon” seamănă cu nucul kremnos - „skel, skel”.
Cuvinte noi care să înțeleagă
- Surse naturale de siliciu: siliciu, cuarț și alte soiuri, silice, aluminosilicat, azbest.
- Semnificația biologică a siliciului.
- Dominanța siliciului: napіvprovіdnikovі, interacțiunea cu acru, metale, pajiști.
- Silane.
- Oxid de siliciu (IV). Yoga Budova și putere: interacțiune cu pajiști, oxizi bazici, carbonați și magneziu.
- Acid silicic și săruri її. Rozchinne slo.
- Zastosuvannya silicon și yogo jumătate.
- Sklo.
- Ciment.
numește ziua
Cel mai adesea, în natură, siliciul se găsește într-un aspect ca silice - o bază pe bază de dioxid de siliciu (IV) SiO 2 (aproximativ 12% din masa pământului de rujeolă). Principalele minerale și roci care sunt stinse de dioxid de siliciu sunt lanț (bogat și cuarț), cuarț și cuarț, silex, polov_spar. Siliciul și aluminosilicatul sunt pliate într-un altul pentru lățimea în natură.
Se remarcă unul câte unul faptul importanței siliciului pur în aspectul său nativ.
Otrimannya
Siliciul va ieși la prăjirea pisku alb crocant (dioxid de siliciu) cu magneziu:
S i O 2 + 2 M g → 2 M g O + Si (\displaystyle ~(\mathsf (SiO_(2)+2Mg\\rightarrow \ 2MgO+Si)))La ce te stabilești siliciu amorf , ce poate arăta ca o pudră maro.
În industrie, puritatea tehnică a siliciului se obține prin topirea SiO 2 cu cocs la o temperatură de aproximativ 1800 ° C în cuptoare minerale-termice de tip arbore. Puritatea siliciului îndepărtat de un astfel de grad poate ajunge la 99,9% (principalele case sunt cărbune, metal).
Vă puteți îndepărta de purificarea siliciului din case.
- Purificarea în toaletele de laborator poate fi efectuată printr-un traseu al posesiei frontale de siliciură de magneziu Mg 2 Si. Am dat siliciur de magneziu pentru acizi clorhidric sau octic suplimentari pentru a îndepărta monosilanul asemănător gazului SiH4. Monosilanul este purificat prin rectificare, sorbție și alte metode și apoi plasat pe siliciu și apă la o temperatură de aproximativ 1000 °C.
- Purificarea siliciului la scară industrială se realizează printr-o cale de clorurare neintermediară a siliciului. Cu aceasta, se dizolvă semipliurile depozitului SiCl 4 , SiHCl 3 și SiH 2 Cl 2 . Їх într-un mod diferit curățați casa (de regulă, prin distilare și disproporționare) și în etapa finală adăugați apă pură la temperaturi de la 900 la 1100 °C.
- Sunt dezvoltate tehnologii industriale mai ieftine, mai curate și mai eficiente pentru purificarea siliciului. Pentru 2010 înaintea acestora este posibil să se introducă tehnologii pentru purificarea siliciului cu fluor indirect (înlocuind clorul); tehnologii care transferă distilarea la monoxid de siliciu; tehnologii bazate pe case cu vitralii care se concentrează pe granițele dintre cristale.
Vmіst domіshok la siliciul finalizat poate fi redus la 10 -8 -10 -6% pe masă. Mai multe rapoarte despre nutriția siliciului pur sunt revizuite în articolul Siliciu policristalin.
Metoda de obținere a siliciului într-o formă pură de fragmentare de Mikola, Mikolayovich Beketov.
Puterea fizică
Rețeaua cristalină de siliciu este centrată pe față cubică ca diamantul, parametrul a = 0,54307 nm (la menghină înaltă elimina alte modificări polimorfe ale siliciului), dar printr-o legătură mai mare între atomii de Si-Si într-o legătură cu o legătură zv'azku S-S duritatea siliciului este semnificativ mai mică decât cea a diamantului. Siliciu trosnind, numai atunci când este încălzit la 800 ° C, devine vorbire plastică. Vіn prozory pentru infrachervonogo viprominyuvannya s dozhini khvili 1,1 microni. Concentrația umedă a nasului în sarcină este de 5,81 10 15 m-3 (pentru o temperatură de 300 K).
Putere electrofizică
Siliciul elementar într-o formă monocristalină este un conductor cu gol indirect. Lățimea zonei împrejmuite la temperatura camerei stocare 1,12 eV, iar la T \u003d 0 K - 1,21 eV. Concentrația purtătorilor de sarcină umedă în siliciu pentru mințile normale devine aproape de 1,5·10 10 cm −3 .
Pe puterea electrotrofică a siliciului cristalin, un mare aflux construiește case care cutreieră în întuneric. Pentru a extrage cristale de siliciu cu o conductivitate profundă, introduceți în siliciu atomi de elemente din grupa III, cum ar fi bor, aluminiu, galiu și indiu. Pentru a extrage cristale din siliciu cu conductivitate electronică la siliciu, introduceți atomi elementele V-ї groupi, cum ar fi fosfor, mish'yak, surma.
Când dispozitivele electronice sunt asamblate pe bază de siliciu, este important să atașați bila de suprafață la material (până la zeci de microni), astfel încât calitatea suprafeței cristalului poate fi adăugată la puterea electrostatică a siliciului și, aparent, asupra puterii instrumentului finit. În cursul asamblarii anumitor dispozitive, se adaugă vicoros, aplicat la modificarea suprafeței, de exemplu, suprafața este acoperită cu siliciu cu diverși agenți chimici și її oprominennya.
Putere chimică
Similar atomilor de carbon, atomii de siliciu sunt caracterizați prin hibridizarea sp 3 a orbitalilor. La legătura cu hibridizarea, siliciul cristalin pur face granule asemănătoare diamantului, în care siliciul este cotivalent. În același timp, sunetul de siliciu se manifestă și ca un element cotivalent cu o stare de oxidare de +4 sau -4. Zustrichayutsya jumătate de siliciu bivalent, de exemplu, oxid de siliciu (II) - SiO.
Pentru mințile normale, siliciul este inactiv din punct de vedere chimic și reacționează activ doar cu fluorul asemănător gazului, cu care se dizolvă tetrafluorura de siliciu volatilă SiF4. O astfel de „inactivitate” a siliciului se datorează pasivării suprafeței bilei de dioxid de siliciu de dimensiuni nanometrice, care se stabilește negativ în prezența apei acru, din nou și din nou (vapori de apă).
acidificarea cu dioxidul de SiO 2 dizolvat, procesul este însoțit de o creștere a volumului bilei de dioxid la suprafață, stabilitatea procesului de oxidare este limitată de difuzia acidului atomic și a dioxidului de crioconservare.
Când este încălzit la o temperatură de peste 400-500 ° C, siliciul reacționează cu clorul, bromul și iodul - cu adoptarea de tetrahalogenuri SiHal 4 ușor volatile și, eventual, de halogenuri într-un depozit pliat.
Cu apă, siliciul fără mijloc nu reacționează, dar cu apă siliciul - silanii cu formula Si n H 2n + 2 - posedă o cale indirectă. Monosilan SiH 4 (yogo este adesea numit simplu silan) este observat în interacțiunea siliciurilor metalice cu acizii, de exemplu:
C a 2 S i + 4 H C l → 2 C a C l 2 + S i H 4 (\displaystyle ~(\mathsf (Ca_(2)Si+4HCl\\rightarrow \ 2CaCl_(2)+SiH_(4))\) ) Săgeata în sus)))SiH 4 silan, care se dizolvă în această reacție, răzbune case și alți silani, zokrem, Si 2 H 6 disilan și Si 3 H 8 trisilan, în unele lancete pentru atomi de siliciu, legați între ele prin legături simple (- Si -Si-Si- ).
Siliciul reacționează cu azotul și borul la temperaturi apropiate de 1000 ° C, dizolvând nitrură de Si 3 N 4 și boruri stabile termic și chimic SiB 3 , SiB 6 și SiB 12 .
La temperaturi de peste 1000 ° C, este posibil să se utilizeze siliciu, care este cel mai apropiat analog de tabelul periodic - carbon - carbură de siliciu SiC (carborundum), care se caracterizează prin duritate ridicată și activitate chimică scăzută. Carborundum este utilizat pe scară largă ca material abraziv. Cu aceasta, totuși, topirea siliciului (1415 °C) poate fi contactată timp de trei ore cu cărbunele având în vedere bucățile mari de grafit sinterizat cu granulație fină de presare izostatică, practic neschimbându-se și neintervinând restul.
Elementele inferioare ale grupului al 4-lea (Ge, Sn, Pb) sunt neacoperite cu siliciu, precum și majoritatea celorlalte metale. Când sunt încălzite cu siliciu și metale, se pot forma jumătățile lor, siliciuri. Siliciurile pot fi împărțite în două grupe: ionic-covalente (silicide de băltoacă, metale din băltoacă-pământ și magneziu de tip Ca 2 Si, Mg 2 Si și in) și asemănătoare metalelor (silicide ale metalelor de tranziție). Siliciurile metalelor active sunt așezate sub diluția acizilor; Siliciurile asemănătoare metalelor au un punct de topire ridicat (până la 2000 °C). Cel mai des sunt folosite depozite de siliciu asemănător metalului Pe mine Si, Pe mine 3Si2, Pe mine 2 Si 3 , Pe mine 5 Si 3 i Pe mine Si 2 . Siliciurile asemănătoare metalelor sunt inerte din punct de vedere chimic, rezistente la acru la temperaturi ridicate.
Este deosebit de important de remarcat faptul că siliciul etanșează suma eutectică, care permite împingerea (topirea) materialelor pentru etanșarea ceramicii ferosilicioase la temperaturi care sunt vizibil mai mici, mai mici decât temperatura de topire a sigiliului și a siliciului.
Când se adaugă SiO 2 la siliciu la temperaturi peste 1200 ° C, oxidul de siliciu (II) - SiO este dizolvat. Acest proces este susținut constant de producerea de cristale prin metode cu siliciu
Siliciul în fruntea viziunilor în 1811. J.Gay-Lussac și L.Tenar la trecerea vaporilor de fluorură de siliciu peste potasiu metal, proteinele nu sunt descrise de ei ca element. Chimistul suedez J. Berzelius în 1823 dându-se o descriere a siliciului îndepărtat de acesta în timpul prelucrării sării de potasiu K 2 SiF 6 cu potasiu metalic la temperatură ridicată. Noul element a fost numit „siliciu” (lat. silex - silex). Numele rusesc „siliciu” a fost introdus în 1834 de chimistul rus Herman Ivanovich Hess. La traducerea altor greci. krhmnoz- Kut, munte.
Cunoașterea naturii, otrimannya:
În natură, siliciul se găsește în dioxid de vibrație și silicați într-un alt depozit. Dioxidul de siliciu natural este mai important sub formă de cuarț, dorind să se folosească și alte minerale - cristobalit, tridimit, balenă, cousite. Siliciul amorf se acumulează în depozitele de diatomee de pe fundul mărilor și oceanelor - aceste depozite s-au decontat cu SiO 2, intrând în depozitul de diatomee și alți ciliați.
Siliciul Vilniy poate fi folosit pentru prăjire cu pisku alb crocant de magneziu, care pentru un depozit de produse chimice poate fi curățat cu oxid de siliciu SiO 2 + 2Mg = 2MgO + Si. În industrie, puritatea tehnică a siliciului se obține prin topirea SiO 2 cu cocs la o temperatură de aproximativ 1800 ° C în cuptoare cu arc. Puritatea siliciului obținută printr-un astfel de rang poate ajunge la 99,9% (principalele case sunt cărbunele, metalul).
Puterile fizice:
Siliciul amorf poate arăta ca o pulbere maro, a cărei grosime este mai densă 2,0 g / cm 3. Siliciu cristalin - gri închis, vorbire cristalină strălucitoare, cristalizată și tare, se cristalizează în diamante. Acesta este un conductor tipic (este mai bine să conduci electricitatea, cauciuc de tip izolator mai mic și mai mare pentru un conductor - mijloc). Siliciu trosnind, numai atunci când este încălzit la 800 ° C, devine vorbire plastică. Cіkavo, scho prosorium silicios la infrachervony viprominyuvannya, începând cu un vânt lung de 1,1 microni.
Putere chimica:
Siliciu slab activ din punct de vedere chimic. La temperatura camerei, reacționează doar cu fluorul asemănător gazului, tetrafluorura de siliciu volatilă SiF 4 se dizolvă la această temperatură. Când este încălzit la o temperatură de 400-500 ° C, siliciul reacționează cu acidul cu dioxidul dizolvat, cu clor, brom și iod - cu tetrahalogenuri dizolvate ușor volatile SiHal 4 . La temperaturi apropiate de 1000 ° C, siliciul reacționează cu azotul pentru a dizolva nitrura Si 3 N 4 cu bor - borură stabilă termic și chimic SiB 3, SiB 6 și SiB 12. Cu siliciu apos, nu reacționează fără probleme.
Pentru gravarea cu siliciu, suma acizilor fluorhidric și acizilor azotic este cea mai utilizată.
Amenajat la pajiști.
Siliciul este caracterizat printr-o etapă de oxidare de +4 sau -4.
Cele mai importante domenii:
Dioxid de siliciu, SiO2- (anhidrida de siliciu) ...
...
Acizi silicici- slab, indistinct, utvoryuyuyutsya atunci când se adaugă acid la dimensiunea silicatului arată ca un gel (vorbire asemănătoare gelatinei). Se știe că H4SiO4 (orto-siliciu) și H2SiO3 (meta-siliciu sau siliciu) variază și se transformă irevocabil în Si02 atunci când sunt încălzite și uscate. Produs solid poros pentru a intra - gel de silice poate fi deschis la suprafață și vicoros ca adsorbant de gaze, agent de uscare, catalizator și catalizator de uzură.
silicat- sarurile acizilor silicici ai bunului (crisilicatii de sodiu si potasiu) nu sunt solubile in apa. putere.
Cascade- analogi ai carbohidraților, silani, cu jumătate de inimă, în unii atomi de siliciu cu o singură legătură, putere yakscho atom silicon z'єdnаnі podvіyny zv'yazkom. Lance și kiltsya sunt folosite în mod similar carbohidraților. Toate puterile pot fi angajate pe cont propriu, pot face vibrații de sumish cu repetare și pot reacționa ușor cu apa.
Zastosuvannya:
Cea mai semnificativă cantitate de siliciu este cunoscută pentru selecția aliajelor pentru aplicarea aluminiului, cuprului și magneziului și pentru selectarea ferosilicidelor, care pot fi importante pentru selectarea oțelurilor și a echipamentelor de încălzire. Cristale de siliciu zastosovuyut baterii Sonyși anexe napіvprovіdnikovih - tranzistori și diode. Siliciul servește și ca sirovină pentru producerea plăcilor de organosiliciu sau siloxani, colorate cu ulei, ulei, materiale plastice și cauciucuri sintetice. Limacși anorganici siliciul vicorist este folosit în tehnologia ceramicii și a oțelului, ca material izolator și p'ezocrystals
Pentru unele organisme, siliciul este un element biogen important. Vіn intra în depozitul colibelor de susținere la roslin și scheletic - la creaturi. Organismele marine – diatomee, alge, radiolarie, bureți – sunt concentrate în suprafețe mari de siliciu. Cifre grozave coada-calului și cerealele se concentrează cu siliciu, în primul negru - bambus și pidrodine asemănătoare orezului, printre care - plantarea orezului. M'yazova țesut al unei persoane pentru a se răzbuna (1-2) 10 -2% siliciu, țesut osos - 17 10 -4%, sânge - 3,9 mg / l. Cu toate acestea, până la 1 g de siliciu poate fi ingerat în corpul unei persoane astăzi.
Antonov S.M., Tomilin K.G.
Universitatea de Stat HF Tyumen, grupa 571.
