Didelė silicio koncentracija. Tu žinai kaip
Procesorius? Pisok? O ką jūs turite su žodžių asociacijomis? O gal Silicio slėnis?
Lyg jo nebūtų, su siliciu šiandien lipdome, o jei reikia žinoti, kas yra Si ir kodėl valgai, prašau katės.
Įėjimas
Būdamas vieno iš Maskvos universitetų „Nanomedžiagų“ specialybės studentas, noriu pažinti jus, brangus skaitytojau, su svarbiausiais mūsų planetos cheminiais elementais. Aš jau seniai rinkausi ką nors, anglį ar silicį, bet vis dėlto nusprendžiau pats naudoti Si, todėl bet kurios šiuolaikinės programėlės esmė yra būtent ji, taigi, galima sakyti, puikiai. Pasistengsiu, kad mano mintys būtų labai paprastos ir prieinamos, parašęs šią medžiagą, ją išsaugojau, daugiausia naujokams, tačiau vis daugiau žmonių gali ją gauti iš cicave, todėl noriu pasakyti, kad straipsnis buvo parašytas išskirtinai interesų plėtrai, kas įstrigo. Taigi pradėkime.
Silicio
Silicis (lot. Silicium), Si, Mendeljevo periodinės sistemos IV grupės cheminis elementas; atominis skaičius 14, atominė masė 28,086.
Gamtoje elementą reprezentuoja trys stabilūs izotopai: 28Si (92,27%), 29Si (4,68%) ir 30Si (3,05%).
Storis (n.s.) 2,33 g/cm?
Lydymosi temperatūra 1688 K

Milteliai Si
Istorinis įrodymas
Silicio kalvos, plačios žemės, žmonių bulvarai iš akmens amžiaus. Ten buvo tūkstančiai akmens šprotų ir akmens laistymo. Zastosuvannya spoluk Silicis, susietas su jų apdorojimu, - sandėlio paruošimas - prasidėjo maždaug 3000 m. pr. Kr. e. (Senasis Egiptas). Anksčiau namuose buvo naudojamas silicis – oksidas SiO2 (silicio dioksidas). 18 amžiuje silicio dioksidas buvo sušvirkščiamas paprastu kūnu ir nešamas į „žemes“ (kas vartojama jo pavadinime). Skladnіst į silicio dioksido sandėlį, įrengus І. I. Berzelius. Vіn pats vpershe, 1825 m., pašalinęs elementarų silicį iš silicio fluorido SiF4, pakeisdamas likusį metalinį kalį. Naujasis elementas buvo pavadintas „silicium“ (lot. silex – titnagas). Rusiškas vardas vvіv G.I. Hessas 1834 m.

Silicio lankas plėtinių gamtoje garso garso sandėlyje
Plečiantis silicis gamtoje
Pagal plotį žemės plutoje silicis yra kitas (po rūgštaus) elementas, jo vidurkis litosferoje yra 29,5% (už masės). Žemės žievė, silicio pilka, atlieka tą patį pagrindinį vaidmenį, kaip ir būtybės žemiškojo pasaulio anglis. Silicio geochemijai ypač svarbu, kad ryšys tarp jogo ir rūgštaus būtų svarbus. Beveik 12% litosferos tampa silicio dioksidu SiO2 mineralinio kvarco ir įvairių atmainų pavidalu. 75% litosferos sudaro įvairūs silikatai ir aliumosilikatai (polova, žėrutis, amfibolinis toščas). Bendras mineralų, kuriuos galima pakeisti silicio dioksidu, skaičius viršija 400.
Fizinė silicio galia
Manau, kad tai ypač ne varto, tai viskas Fizinė galia Turiu nemokamą prieigą, bet išvardinsiu dažniausiai pasitaikančius.
Virimo temperatūra 2600 °С
Silicio prozoriumas dovgokhvilovyh ІCh-promenіv
Dielektrinis skverbtis 11.7
Moso silicio kietumas 7.0
Norėčiau pasakyti, kad silicio tenditny medžiaga, proginė plastinė deformacija prasideda aukštesnėje nei 800°C temperatūroje.
Silicis yra laidininkas, tas pats vynas, kurį žinome daug zastosuvannya. Silicio elektros galia gali slypėti namuose.
Cheminė galia.
Čia turtinga, nuostabu, galima sakyti, bet aš užkliūvau už garsiausio. Si lentynose (panašiai į anglį) 4-valentas.
Silicio zavdyak paviršiuje oksido lydymas yra stabilus vėjui esant aukštesnei temperatūrai. Rūgštyje jis oksiduojasi 400 °C temperatūroje, ištirpindamas silicio oksidą (IV) SiO2.
Silicis atsparus rūgštims ir rečiau maišomas su azoto ir fluoro rūgštimis, lengvai atskiriamas karštose pievose nuo matomo vandens.
Silicis sudaro 2 rūgščių silanų grupes – siloksaną ir siloksenį. Silicis reaguoja su azotu aukštesnėje nei 1000 °C temperatūroje. tai vertinga medžiaga chemijos pramonei, taip pat gesintuvų gamybai. Didelio kietumo, taip pat šiluminio ir cheminio atsparumo, yra apdorojamos silicio karbido (silicio karbido SiC) ir boro (SiB3, SiB6, SiB12) grindys.
Otrimanya silicis
Manau, tse naytsіkavіsha dalis, čia yra ataskaita.
Atpažinimo tipas yra padalintas:
1.
Silicio elektroninė galia(t.z. elektroninis silicis"") - silicio dulksnos silicio rūko viršija 99,999% už sienos silicio, silicio elektroninės kokybės elektrinė atrama gali būti keičiama maždaug nuo 0,001 iki 150 omų cm intervalu, bet su kuriuo atramos vertė kaltas buti aprūpinamas viskas įskaičiuota namais, kad galėtum patekti į kitų namų krištolą, norintis pasirūpinti darželio elektros opir užduotimis, skambėti, nepriimtina.
2.
Silicio sony kokybė(t.z. "sonyachny silicon") - silicis iš mišraus silicio daugiau nei 99,99% viename pluošte, kuris naudojamas fotoelektrinių konvertavimo įrenginių (garso baterijų) gamybai.

3.
Techninis silicis- polikristalinės silicio struktūros blokai, paimti karboterminio atnaujinimo būdu iš gryno kvarco girgždesys; danga 98% silicio, pagrindinis namas anglis, vėdinamas dideliu kiekiu lengvųjų elementų - boro, fosforo, aliuminio; daugiausia naudojamas polikristaliniam siliciui laikyti.
Techninio grynumo silicis (95-98%) turi elektrinius įkvėpto silicio dioksido SiO2 sprogimus tarp grafito elektrodų. Ryšium su nap_v_dnikovoї tehnіko razrobleno gryno ir ypač gryno silicio gavimo metodo kūrimu. Dėl gryno vih_dnih spoluk silicio, z yakikh vityagyat silіkі vіdnovlennya vіdnovlennya аbo termіchnogo razkladannya sintezės.
Polikristalinis silicis ("polisilicis") - gryniausia silicio forma, kuri yra komerciškai perspektyvi, - produktas, naudojamas techninio silicio valymui chlorido ir fluorido metodais ir yra pergalingas mono- ir daugiakristaliniam silicio gamyboje. silicio.
Tradiciškai polikristalinis silicis pašalinamas iš techninio silicio, perkeliant jogą į silanų (monosilano, chlorsilano, fluorosilano) čiaupus su įžeidžiančiu silanų dugnu, kurie nusėda, rektifikuojamas konvertuoto silano valymas ir silano atnaujinimas į metalinį silicį. .
Gryno silicio laidininkai gaunami dviejų tipų: polikristalinis(SiCl4 arba SiHCl3 sutvirtinimas cinku arba vandeniu, šiluminis SiI4 ir SiH4 plėtimasis) ir monokristalinis(Tiglių neturinčios zonos lydymas ir vieno kristalo „apvijimas“ iš išlydyto silicio - Czochralsky metodas).

Čia galite naudoti Czochralski metodą vibruoti siliciui.
Czochralskio metodas- kristalų vibravimo būdas vingiuoti į kalną ore ant didelio įsipareigojimo lydyti paviršiuje, prasidėjus kristalizacijos burbuolei, atnešant pradinį kristalą (arba didelį kristalų skaičių). ) tam tikros struktūros ir kristalografinės orientacijos atsії liečiantis su laisvu paviršiaus lydalu.
Zastosuvannya silicis
Specialiai legiruotas silicis plačiai naudojamas kaip medžiaga elektros laidininkams (tranzistorių, termistorių, galios vibratorių, tiristorių, sony fotoelementų, kurie naudojami erdvėlaiviuose, taip pat daug visokių dalykų) ruošimui.
Silicio prosoria skeveldros, skirtos pakeisti nuo 1 iki 9 mikronų ilgių plaukų, gali būti dedamos į infraraudonųjų spindulių optiką.
Silicis gali būti skirtingas ir visos zastosuvannya sritys, kurios plečiasi. Metalurgijoje Si
vikoristovuetsya rūgštingumo pašalinimui (deoksidacijai) iš lydytų metalų.
Silicis sandėlį daug salės ir spalvotų metalų lydinių.
Sound Silicio lydiniai, skirti padidinti atsparumą korozijai, pagerinti jų galią ir padidinti mechaninį stiprumą; prote su didesniu zmistі Silicio gali viklikati kryhkіst.
Svarbiausi yra lydiniai, vario ir aliuminio lydiniai, kuriais galima atkeršyti diržus.
Silicio dioksidas apdorojamas stiklo, cemento, keramikos, elektros ir kitomis pramoninėmis galuzomis.
Silicio valymas yra svarbus gaminant atskirus elektroninius prietaisus (pavyzdžiui, kompiuterio procesorių) ir vieno lusto mikroschemas.
Grynas silicis, naudojamas grynam siliciui, metalurginio silicio valymas, nes kristalinis silicis yra pagrindinė sony energijos žaliava.
Vieno kristalo silicis – elektronikos ir sony energetikos kremas naudojamas dujinių lazerių veidrodžiams gaminti.

Valomasis silicis ir jogos gaminys
Silicis kūne
Silicio kūne randama įvairių spolukų akyse, kurios užima pirmaujančią vietą apšviečiant kietas skeleto dalis ir audinius. Ypač daug silicio gali kauptis jūros dumblių (pavyzdžiui, diatomitinių dumblių) ir būtybių (pavyzdžiui, silicio rago kempinės, radiolarijos), kurios tuo metu, kai vandenynas vandenyno dugne, sukietėja dėl silicio oksido nuosėdų. (IV). Šaltose jūrose ir ežeruose svarbesni yra biogeniniai mulai, kuriuose gausu silicio, tropinėse jūrose - garuojantys mulai, kuriuose mažai silicio. Daug silicio antžeminių ataugų viduryje sukaupia žolės, viksvos, palmės, asiūkliai. Stuburo būtybėse vietoj silicio (IV) oksido, pelenų upėse 0,1-0,5 proc. Daugiausiai silicio pasireiškimų šarminėje laimingas audinys, nirkah, pidshlunkovy skliautas. Papildomoje dietoje žmonės turi iki 1 g silicio. Į orą patekus daug silicio (IV) oksido, jis sunaudojamas žmogaus, sukeliančio ligą – silikozę, legenijoje.
Visnovok
Na, o nuo visko, jei perskaitėte iki galo ir šiek tiek įsiskverbėte, vadinasi, esate šiek tiek arčiau sėkmės. Aš spodіvayus, rašydamas aš ne veltui ir pіst vouchsafed į hoch komu. Už pagarbą.
SILIKONIS. (Silicio), Si - chem. periodinės elementų sistemos grupės IV elementas; adresu. n. 14, val. m. 28,086. Kristalinė silicio tamsiai pilka kalba su dervingu blizgesiu. Daugeliu atvejų atskleidžiamas oksidacijos laipsnis - 4, +2 ir +4. Natūralus silicis sudarytas iš stabilių izotopų 28Si (92,28%), 29Si (4,67%) ir 30Si (3,05%). Radioaktyviųjų izotopų 27Si, 31Si ir 32Si pašalinimas su atvirkštinio skilimo periodais 4,5 sekundės, 2,62 metų ir 700 metų. pirmą kartą pamatytas 1811 m. prancūzų kalba. chemikas ir fizikas J. L. Gay-Lussac ir prancūzas. chemikas L. J. Tenaras, tačiau identifikacijų yra mažiau 1823 m Švedas, chemikas ir mineralogas J. Ya. Berzelius.
Už plotį žemės plutoje (27,6%), silicis-kitas (po rūgštaus) elementas. Svarbu žinoti. silicio dioksido Si02 ir kitų rūgščių kalbų pavidalu (silikatai, aliumosilikatai ir kt.). Geriausiems protams yra sukurta stabili servetėlės modifikacija, kurios kubinė struktūra yra į veidą kaip deimantas, kurios periodas a = 5,4307 A. Protarpinis įsiskverbimas yra 2,35 A. Plotis yra 2,328 gcm. Esant aukštam slėgiui (120-150 kbar) pereikite prie didesnių laidų ir metalinių modifikacijų. Metalo modifikacija-superlaidininkas, kurio pereinamoji temperatūra 6,7 K. Didėjant slėgiui, lydymosi temperatūra sumažėja nuo 1415 ± 3 ° C esant 1 bar slėgiui iki 810 ° C esant 15 104 barų slėgiui retai). ). Kai lydosi, padidėja tarpatominių ryšių koordinavimo skaičius ir metalizacija. Amorfinis silicio charakteristika trumpo nuotolio tvarka, kuri rodo stipriai sukurtą į tūrį orientuotą kubinę struktūrą, artimą retam. Debievskaja t-ra yra arti 645 K. Koef. temperatūros tiesinis plėtimasis keičiasi kintant t-ri pagal kraštutinį dėsnį, mažesnis nei t-ri 100 To vynas tampa neigiamas, pasiekdamas minimumą (-0,77 10 -6) laipsnį -1 esant t-ri 80 K; esant t-rі 310 K vynas yra 2,33 10-6 laipsnis-1, o t-rі 1273 K-4,8 10 laipsnių-1. Lydymosi šiluma 11,9 kcal/g-atomas; tkіp.3520 K.
Sublimacijos ir garavimo šiluma lydymosi temperatūroje yra 110 ir 98,1 kcal/g-atomas. Silicio šilumos laidumas ir elektrinis laidumas priklauso nuo kristalų grynumo ir kruopštumo. Zі rostannyam t-ri koef. gryno K. šilumos laidumas laipsniškai didėja (iki 8,4 cal/cm X X sek deg, esant t-ri 35 K), o po to kinta, pasiekdamas 0,36 ir 0,06 cal/cm s t-ri vіdpovidno 300 ir 1200 K. Entalpija, entropija ir šiluminė talpa K. standartiniu požiūriu lygi 770 cal/g-atom, 4,51 ir 4,83 cal/g-atom - deg. Silicio diamagnetinis, kieto (-1,1 10 -7 mu/g) ir reto (-0,8 10 -7 mu/g) magnetinis jautrumas. Silicis silpnai nusėda t-ri. Reto K. paviršiaus energija, storis ir kinematinė klampumas lydymosi temperatūroje tampa 737 erg/cm2, 2,55 g/cm3 ir 3 10 m2/sek. Tipiškas kristalinio silicio laidininkas, kurio aptvertos zonos plotis yra 1,15 ev, esant t-p 0 iki 1,08 u - esant t-p 300 K. Kambario temperatūroje šlapią nešančių krūvių koncentracija yra artima 1,4 10 10 cm - 3;
Silicio galia kristi dėl namų prigimties ir koncentracijos, taip pat dėl kristalo tobulumo. Žiedas otrimannya napіvprovіdnikovogo Do. vykdant r ir n tipo jogą, jie derinami su IIIb (boras, aliuminis, galis) ir Vb (fosforas, mišjakas, stibis, bismutas) pogrupiu, kurie sukuria sukupnіst vіdpovіdno akceptoriui ir donorui rіvnі , roztashovannyh šalia zonų kordonų. Vikoristo legiravimui tie kiti elementai (pavyzdžiui) formuojami taip. glybokі rivnі, yakі obumovlyuyut laidojimo ir rekombinacija nosesіїv mokesčius. Tse leidžia paimti medžiagas su dideliu elektros kiekiu. atrama (1010 omų cm esant t-rі 80 K) tą mažą smulkaus susidėvėjimo krūvio pagrindo trivalumą, kuris yra svarbus įvairių ūkinių pastatų skaičiaus didėjimui. Koeficientas termoelektrinė galia su siliciu tiesiog turi būti nusodinta į t-ri ir namo vietoje, zbіlshyuyuchi zі zrostannym elektroopor (esant p = 0,6 omo - cm, a = 103 mikrovoltai / kruša). Silicio dielektrinis įsiskverbimas (vіd 11–15) yra silpnai nusėdęs sandėlyje ir monokristalų kruopštumas. Silicio optinio molio dėsniai labai keičiasi dėl grynumo, koncentracijos ir gyvenimo defektų pobūdžio pasikeitimo bei ilgaamžiškumo.
Elektromagnetinio kolivano netiesioginio molio kordonas artėja prie 1,09 euro, tiesioginio – iki 3,3 euro. Matomoje kompleksinio lūžio rodiklio (n - ik) parametrų spektro srityje jau galima gulėti ant namo paviršiaus. Ypač grynam Do. (atλ \u003d 5461 A ir t-re 293 K) n \u003d 4,056 ir k \u003d 0,028. Roboto elektronikos išeiga – arti 48 eurų. Silicio tendencija. Jogo kietumas (t-ra 300 K) Moosui - 7; HB = 240; HV y \u003d 103; I = 1250 kgf / mm2; normų modulis, tamprumas (polikristalinis) 10890 kgf/mm2. Tarp minerališkumo gulėti kristalo gylyje: ant vigino gylis yra nuo 7 iki 14; koef. Standumas 0,325 1066 cm2/kg.
Kambario temperatūroje silicis praktiškai nesąveikauja su dujiniais (įskaitant) ir kietais reagentais, krіm lіv. Judant t-ri, vyksta aktyvi sąveika su metalais ir nemetalais. Zocrema, kuri tirpina SiC karbidą (1600 K temp.), Si3N4 nitridą (1300 K temp.), fosfidą SiP (1200 K temp.) ir arsenidą Si As, SiAS2 (1000 K temp.). Su rūgštine reakcija 700 K temperatūroje, gesinant Si02 dioksidą, su halogenais - SiF4 fluoridu (esant aukštesnei kaip 300 K temperatūrai), SiCl4 chloridui (esant aukštesnei nei 500 K temperatūrai), SiBr4 bromidui (esant 700 K) i mazgas SiI4 (esant 1000 mp). Intensyviai reaguoja su daugeliu kitų. metalai, nustatantys tvirtus skirtumus jų pakeitime chi chem. pusėje - silicidai. Kietųjų rožių homogeniškumo koncentracijos sritys atsiranda priklausomai nuo rozetės pobūdžio (pavyzdžiui, Nimechchine nuo 0 iki 100%, rudenį iki 15%, alfa cirkonyje mažiau nei 0,1%).
Skirtumas tarp metalų ir nemetalų kietajame silicyje yra žymiai mažesnis ir skamba retrogradiškai. Su kokiomis sienomis, o ne namu, kas daroma Do. nelabai giliai, pasiekite maksimumą ( 2 10 18 , 10 19 , 2 10 19 , 1021 , 2 10 21 cm) plotas t-r vіd nuo 1400 iki 1600 K. Namai su giliu vіdznyayutsya šiek tiek mažesniu rozchinnіstyu (vіd 1015 selenui ir 5 10 16 zalіza iki 7 10 17 nikelio ir 10 18 cm-3 midi). Retame pliene silicis nėra apsuptas paprastų metalų, dažnai su dideliu karščio regėjimu. Grynas silicis ruošiamas iš techninio produkto 99% Si і - 0,03% Fe, Al і Co), grūdintas kvarcu ir anglimi elektrinėse krosnyse. Pradėkite nuo naujo kvėpavimo į ten (sum_shy druskos ir sirchanoy, o paskui fluoro-vandens ir sirchanoy) namus, po kurių produktas (99,98%) paimamas, apdorojamas chloru. Sintezės išvalomos distiliuojant.
Silicio laidininkas naudojamas kartu su SiCl4 chloridu (arba SiHCl3) vandenyje arba šiluminiam SiH4 hidrido plėtimuisi. Likutinis monokristalų valymas ir malimas atliekamas betiglio zonos lygiuoju metodu arba Czochralsky metodu, atsižvelgiant į ypač gryną padažą (namuose iki 1010-1013 cm-3) cf\u003e 10 3 omų cm. iv esant kurioms įvesti reikiamų namų skaičiaus dozavimą. Taip ruošiate 2-4 skersmens ir 3-10 cm ilgio cilindrinius kremus Specialiems. Tikslas yra pagaminti dar daugiau monokristalų. Techninis silicis ir ypač jogo lydiniai iš fiziologinio tirpalo, pavyzdžiui, rūgštinio plieno ir lydinių, taip pat lengvi priedai. Ypatingai grynas zrazki monokristalinis K., legiruotas įvairiais elementais, yra žinomas kaip įvairių silpnų srovių (zocrema, termoelektrinių, radijo, šviesos ir fototechninių) ir aukštos srovės (vibracinių, konvertuojančių) priedų pagrindas.
Silicis ir silicis
Silicis atnešamas į nemetalus, o 4 elektronai gali būti tame pačiame energijos lygyje. Vіn gali vіddavati їх, rodydamas oksidacijos stadiją + 4 ir pridėti elektronų, rodydamas oksidacijos stadiją - 4. Tačiau galimybė pridėti elektronų į silicį yra žymiai mažesnė, mažesnė nei anglies. Silicio atomai gali turėti didesnį spindulį, mažesnius anglies atomus.
Gamtos žinios apie silicį .
Silicio prailginimo arka gamtoje. vienai її kritimo taško daliai daugiau nei 26% masės žemės tymų. Dėl vynų pločio sėdėkite kitoje vietoje (po rūgštumo). Ant vіdmіnu vіd vіd uglec C vіlny stіnі vіrіdі ne zustrichaetsya. Į sandėlį patenka įvairios cheminės sudėties, daugiausia įvairių modifikacijų silicio oksido (IV) ir silicio rūgščių druskų (silikatų).
Manija su siliciu .
Techninio grynumo (95 - 98%) pramoninės klasės silicyje dominuoja SiO 2 koksas elektrinėse orkaitėse skrudinant:
SiO 2 + 2C \u003d Si + 2CO
SiO 2 + 2Mg \u003d Si + 2MgO
Tokiu būdu iš namų paimami rudos spalvos amorfiniai silicio milteliai. Rekristalizacija iš lydančių metalų (Zn, Al) gali būti perkelta į kristalų malūną.
Silicio tetrachloridas, net ir labai grynas, naudojamas 1000 °C temperatūroje silicio tetrachloridui SiCl. 4 poros cinko:
SiCl 4 + 2Zn \u003d Si + 2ZnCl 2
kad valymo jogas laikantis specialių metodų.
Fizinis Cheminė galia silicio.
Grynas kristalinis silicis – tendencingas ir kietas, suglebęs nuolydis. Kaip ir deimantas, jis turi kubinę kristalinę gardelę su kovalentiniu ryšiu. Jogo lydymosi temperatūra 1423 °C. Didžiausiems protams silicio neaktyvus elementas, kuris reaguoja tik su fluoru, bet kaitinamas įsitraukia į įvairias chemines reakcijas.
Yogo vikoristovuyut kaip vertinga medžiaga napіvprovіdnikovіy tehnіtsі. Suporuotas su kitais vyno laidininkais, jis išsiskiria dideliu atsparumu praskiestoms rūgštims ir puikia elektrine varža iki 300 °C. Techninis silicis ir ferosilicio vikoristas taip pat metalurgijoje, skirtas karščiui, rūgštims atspariems ir įrankių plienams, čavunams ir kitiems turtingiems lydiniams.
Su silicio metalais chemijos, Vadinami silicidais, kaitinant su magniu, magnio silicidas ištirpsta:
Si + 2Mg = Mg 2 Si
Metalų silicidai, esantys už tos dominavimo struktūros, prognozuoja karbidus, todėl į metalus panašūs silicidai, kaip ir į metalą panašūs karbidai, išsiskiria dideliu kietumu, aukšta lydymosi temperatūra, karštu elektriniu laidumu.
Kepant sumišą su koksu elektrinėse krosnyse silicio karbidas ir anglis sumaišomi su silicio karbidu arba karborundu:
SiO2 + 3C = SiC + 2CO
Karborundas yra ugniai atspari, kieta kalba be barų, vertinga abrazyvinė ir šiluminė medžiaga. Karborundas, jakas i, maє atominis kristalinis nemokamas. Prie švarios stoties yra izoliatorius, bet esant namui, jis tampa laidininku.
Silicio jakas i , tirpina du oksidus: silicio oksidą (II) SiO ir silicio oksidą (IV) SiO 2 . Silicio oksidas (IV) yra kieta ugniai atspari kalba, plačiai paplitusi laisvoje šalyje. Tai chemiškai stabili kalba, kuri sąveikauja tik su fluoru ir į dujas panašiu fluoru vandenyje arba vandenilio fluorido rūgštyje:
SiO 2 + 2F 2 \u003d SiF 4 + O 2
SiO 2 + 4HF \u003d SiF 4 + 2H 2 O
Nurodymas tiesiai į reakcijas paaiškinamas tuo, kad silicis gali turėti didelį sporingumą fluorui. Be to, silicio tetrafluoridas yra skraidanti kalba.
Tuo tekhnіtsі prozoriya SiO 2 vykorovuyut stabilios ugniai atsparios kvarco plokštės paruošimui, nes maloniai praleidžia ultravioletinių spindulių kaitą, gali turėti didelį plėtimosi koeficientą, kuris parodo didelius temperatūros pokyčius. Amorfinė silicio oksido (II) tripolio modifikacija turi didelį poringumą. Yogo vikoristovuyut kaip šilumos ir garso izoliatorius vibruojančiam dinamitui (nosies vibukhovo kalba) ir pan. Silicio (IV) oksidas vibraciniame garse yra vienas iš pagrindinių kasdieninės medžiagos. Jis yra svarbus gaminant ugniai ir rūgštims atsparias medžiagas, plieną, kaip srautas metalurgijoje ir pan.
Pagal molekulines formules anglies oksido (IV) ir silicio oksido (IV) cheminę ir fizinę galią lengva suderinti, jų galia yra panaši chemijos sandėlis z'ednan raznі. Kodėl aiškinama, kad silicio oksidas (IV) susidaro ne tik iš SiO molekulių 2 , pavyzdžiui, s їх asocijuotų, kai kuriuose iš jų silicio atomai yra sujungti rūgštaus atomais. Silicio (IV) oksidas (SiO 2 )n. Vaizdas її aikštėje:
Kitas D. I periodinės sistemos IV grupės (IVA grupės) galvos pogrupio elementų atstovas. Mendelijevas – silicis Si.
Gamtoje silicis yra dar vienas cheminis rūgšties pločio elementas. Žemės pluta vis dažniau kas ketvirtį susilanksto iš yogo spoluko. Labiausiai paplitęs silicis yra silicio oksidas (IV) SiO 2, kitas pavadinimas yra silicio dioksidas. Gamtoje vynai gaminami naudojant mineralinį kvarcą (mažas 158), gausią įvairovę tokio – girsky krištolo, taip pat garsiosios alyvinės formos – ametisto, taip pat agato, opalo, jaspio, chalcedono, karneolio pavidalo. virobnі ir svaiginantys akmenys. Silicio (IV) oksidas taip pat sudarytas iš nuostabaus kvarcinio smėlio.

Mal. 158.
Kvarco kristalai įsiterpę į dolomitą
Trys skirtingi mineralai silicio oksido (IV) pagrindu (titnagas, chalcedonas ir kt.) pirmieji žmonės paruošta znaraddya pracі. Tas pats titnagas, kuris yra nepastebimas ir ne siauresnis už akmenį, klojantis akmens burbulą vіtsі - vіtsі kremіnyh znaryad pratsі (159 pav.). Tam yra dvi priežastys: titnago plotis ir prieinamumas, taip pat pastatų, kurių kraštai yra aštrūs, statyba.

Mal. 159.
Znaryaddya akmuo vіku
Kita natūralių medžiagų rūšis siliciui yra silikatas. Tarp jų yra didžiausi aliuminio silikatų pločiai (buvo suprasta, kad šie silikatai gali pakeisti aliuminio cheminį elementą). Granitas dedamas į aliumosilikatus, matyti kitaip molis, žėrutis. Silikatas, kuris nekeršija aliuminio, pavyzdžiui, asbestas, naudojamas fejerverkams gaminti.
Silicio oksidas (IV) SiO 2 yra būtinas augintojų ir būtybių gyvybei. Vynai suteikia roslin stiebams ir zahisnymi būtybių šydus (160 pav.). Zavdyaki yomu eilės, eilės ir asiūkliai stovi mitzno, kaip maišeliai, gostre lapuojančios viksvos, supjaustytos, kaip peiliai, ražienas ant nuožulnaus lauko, kaip galva, ir javų stiebai ant mitznos grindų, kurie neleidžia laukuose javų laukų. gulėti lentoje ir vėjyje . Luska šonkaulis, komos kriauklės, krilių meteliks, pir'ya ptahiv і mіtsnі būtybių vilna, oskіlki smite silicio dioksidas.

Mal. 160.
Silicio (IV) oksidas suteikia minerališkumo roslino stiebams ir dusinančiosioms būtybių kreivėms
Silicis Z'ednannya suteikia glotnumo ir švelnumo žmogaus plaukams ir nagams.
Silicis patekti ir į sandėlį žemesniųjų gyvų organizmų – diatomų ir radiolarijų, žemiausių gyvosios medžiagos krūtų, tarsi su siliciu sukuriant jų netobulumus už skeleto grožio (161 pav.).
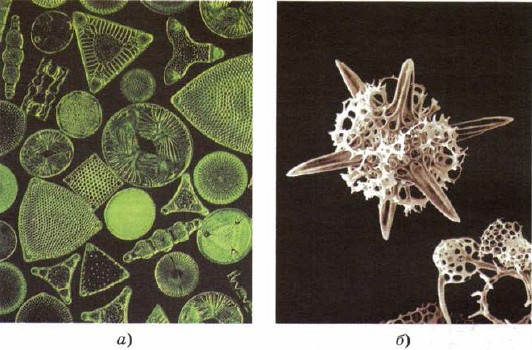
Mal. 161.
Diatomų (a) ir radiolarijų (b) skeletai sudaryti iš silicio dioksido
Silicio dominavimas. Naudojate mikroskaičiuotuvą su „Sony“ baterija, todėl yra pranešimas apie kristalinį silicį. Tse napіvprovіdnik. Ant vіdmіnu vіd metalіv, іz pіdvishennyam temperatūros yogo elektroprovіdnіst zbіshuєtsya. Palydovuose, erdvėlaiviuose, stotyse ir dahah budinkiv (maži 162) jie montuoja „Sony“ baterijas, kurios „Sony“ energiją paverčia elektra. Smarvė veikia kristalai napіvprovіdnikіv, o pirmas juodas titnagas. Silicio fotoelementai gali būti paverčiami elektra iki 10 % molio sony energijos.

Mal. 162.
Mieguistas dahu kabinos akumuliatorius
Silicis deginamas esant rūgštingumui, patenkinantis silicio oksidu (IV):
![]()
Silicis, būdamas nemetalas, kaitinant susilieja su metalais su silicido tirpalais, pavyzdžiui:
![]()
Silicidai lengvai pasiskirsto vandeniu ar rūgštimis, kai matote į dujas panašų į vandenį silicį – silaną:
Ant angliavandenių paviršiaus silanas savaime susijungia ir dega ištirpusiu silicio oksidu (IV) ir vandeniu:
Padidėjusi reakcija tarp silano ir metano CH 4 paaiškinama tuo, kad silicio atomo plėtimasis yra didesnis, mažesnis ties anglimi, todėl Si-H cheminiai ryšiai yra mažesni, CH jungtys yra mažesnės.
Silicio sąveika su koncentruotais vandens pokyčiais pievose, todėl silikatas ir vanduo:
Turi silicio, panašiai kaip silicio oksido (IV) magnio arba anglies:
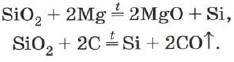
Silicio oksidas (IV), arba silicio dioksidas, arba silicio dioksidas SiO 2 jakas і CO 2 є rūgštinis oksidas. Tačiau CO2 paviršiuje yra molekulinė, bet atominė kristalinė gardelė. SiO 2 yra kieta ir ugniai atspari kalba. Vynai nesiskiria vandens rūgštimis, vandenilio fluorido kremu ir alijošiumi aukštoje temperatūroje pievose su ištirpusiomis silicio rūgšties druskomis - silikatais:
Silicio dioksidas taip pat gali būti naudojamas silicio oksidui (IV) legiruoti su metalų oksidais arba karbonatais:
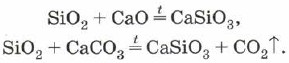
Natrio silikatai ir kalis vadinami mažmeninės prekybos plokštėmis. Їх vandens tiekimas- Gerai naudoti silikatinius klijus.
Silicio rūgštis H 2 SiO 3 (163 pav.):
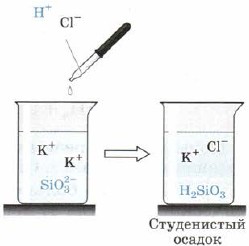
Mal. 163. Rūgštinė reakcija į silikato joną
Be to, H2SiO3 taip pat yra silpna rūgštis. Vandenyje jis nenuoseklus ir iškrenta iš reakcingos suirutės žiūrėdamas į apgulties nuotrupas, kurios kartais suspaudžia visą skirtumo tūrį, paversdamos jį vientisa mase, einu į želė, želė. Pakabinant masi, susidaro labai porėta kalba - silikagelis, kuris plačiai naudojamas kaip adsorbentas - kitų kalbų molis.
Laboratorijos pažyma Nr.40
Silicio rūgšties turėjimas ir tas valdžios patvirtinimas
Silicio įpurškimas. Jau žinote, kad silicis naudojamas laidžioms medžiagoms, taip pat rūgštims atspariems lydiniams gaminti. Kai kvarcinis smėlis sulydomas su vilna aukštoje temperatūroje, ištirpsta silicio karbidas SiC, kuris yra prieinamas tik deimantams. Todėl būtina vicorate už galandimo riztsіv metalorіzalnyh verstatіv ir poliravimo brangus akmuo.
Iš lydyto kvarco ruošiami įvairūs cheminio kvarco indai, kurie gali atlaikyti aukštą temperatūrą, o šalti netrūkinėja.
Silicis Z'ednannya yra sandėlio deformavimo į cementą pagrindas.
Zvichayne klaida gali būti sandėlyje, kurią galima išreikšti formule Na 2 O CaO 6SiO 2. Jogas laimi specialiose krosnyse su lydytu sumish soda, vapnyak ir piska.
Vіdmіnna ryžių skla - zdatnіst rozm'yakshuvatisya і išlydyto plieno išsipūtimo ar tai forma, nes ji išsaugoma, kai sandėlyje yra sugauti. Jo pagrindu gaminami indai ir kiti dirbiniai.
Dodatkovі yakosti sklu duoti įvairių priedų. Taigi švino oksido įvedimas sumažinamas iki skaidrios spalvos, chromo oksidas tampa žalios spalvos, kobalto oksidas yra mėlynas ir tt (164 pav.).

Mal. 164.
Gaminiai iš spalvų sandėlio
Sklo yra vienas seniausių žmonių vyndarių. Jau 3-4 kukmedis. Dėl šios priežasties karas kilo Egipte, Sirijoje, Finikyje ir Juodojoje jūroje.
Sklo - ta pati medžiaga yra ne mažesnė nei remіsnikіv, bet ir menininkai. Maister pasiekė aukščiausią tobulumo lygį Senovės Roma, tarsi jie galėtų atimti savo mozaikų spalvų nuolydį ir darbą.

Mal. 165.
Spalvoti stiklai prie vitražų Notre Dame katedros, Chartres
Kurti meno kūrinius iš sandėlio su obov'yazkovymi atributika puikus muziejus, ir spalvingi vitražai bažnyčios, mozaikinės plokštės - šviesus užpakalis šio (165 pav.). Vienoje iš Rusijos mokslų akademijos Sankt Peterburgo filialo patalpų yra mozaikinis Petro I, pergalingo M. V. Lomonosovo portretas (166 pav.).

Mal. 166.
Mozaikinis Petro I portretas
Spūstys yra gana didelės. Tse vikonne, plyashkove, lampov, dzerkalne sklo; optinis nuolydis - nuo okuliarų iki fotoaparato akinių; niekuo neišsiskiriančių optinių prietaisų lęšiai – nuo mikroskopų iki teleskopų.
Antra pagal svarbą medžiaga – dangos silicio pagrindu – yra cementas. Yogo naudojamas molio ir vape kepimui specialiose krosnyse, kurios yra suvyniotos.
Jei cemento milteliai sumaišomi su vandeniu, tada cementas nėra tvirtai įsitvirtinęs, kitaip, kaip vadinama žadintuvais, cemento rozchinas, kuris žingsnis po žingsnio yra kietesnis. Dedant betoną į cementą ar skaldą, betoną reikia nuimti kaip viršutinį sluoksnį. Betono medžiagiškumas auga, kad į naują įvedamas naujas karkasas - išeina liejamas betonas, iš kurio gaminamos plokštės sienelės, perlaidų blokai, fermi tilteliai ir kt.
Sandėlis užsiima cemento gamyba silikato pramonė. Vaughn taip pat gamina silikatinę keramiką – ceglu, porcelianą (mažą 167), fajansą ir gaminius iš jų.

Mal. 167.
Porceliano veislės
Vidkrittya silicis. Nors senovėje žmonės buvo plačiai naudojami naudojant silicį, patį silicį 1824 m. pirmą kartą atėmė švedų chemikas J. Ya. Berzelius. Tačiau likus 12 metų iki naujojo titnago, J. Gay-Lussac ir L. Tenard buvo atimti, ale vin duzhe zabrudneniy namai.
Lotyniškas pavadinimas silicum kilęs iš lotyniško žodžio silex-titnago. Rusiškas pavadinimas „silicis“ primena riešutmedžio kremnos – „skel, skel“.
Nauji žodžiai, kurie supranta
- Natūralūs silicio šaltiniai: silicio dioksidas, kvarcas ir kitos rūšys, silicio dioksidas, aliumosilikatas, asbestas.
- Biologinė silicio reikšmė.
- Silicio dominavimas: napіvprovіdnikovі, sąveika su rūgščiomis, metalais, pievomis.
- Silanas.
- Silicio (IV) oksidas. Joga Budova ir galia: sąveika su pievomis, baziniais oksidais, karbonatais ir magniu.
- Silicio rūgštis ir її druskos. Rozchinne slo.
- Zastosuvannya silicis ir jogo pusė.
- Sklo.
- Cementas.
pavadink dieną
Dažniausiai gamtoje silicis randamas panašus į silicio dioksidą – pagrindą, kurio pagrindą sudaro silicio dioksidas (IV) SiO 2 (apie 12 % žemės tymų masės). Pagrindiniai mineralai ir uolienos, kuriuos gesina silicio dioksidas, yra grandinės (turtingas ir kvarcas), kvarcas ir kvarcitas, titnagas, polov_spar. Silicio dioksidas ir aliuminio silikatas yra sulankstyti į kitą, kad būtų platesnis gamtoje.
Vienas po kito pažymima gryno silicio svarba jo natūraliai išvaizdai.
Otrimannya
Silicis išsiskirs kepant traškią baltą pisku (silicio dioksidą) su magniu:
S i O 2 + 2 M g → 2 M g O + Si (\displaystyle ~(\mathsf (SiO_(2)+2Mg\ \rightarrow \ 2MgO+Si)))Prie ko tu atsiskaitai amorfinis silicis , kas gali atrodyti kaip rudi pudra.
Pramonėje silicio techninis grynumas gaunamas lydant SiO 2 su koksu maždaug 1800 ° C temperatūroje veleno tipo rūdos šiluminėse krosnyse. Tokia rūšimi pašalinto silicio grynumas gali siekti 99,9% (pagrindiniai namai yra anglis, metalas).
Galite atsisakyti silicio valymo iš namų.
- Valymas laboratorijų prausyklose gali būti atliekamas naudojant magnio silicido Mg 2 Si priekinį kelią. Mes davėme magnio silicidą papildomoms druskos arba oktano rūgštims, kad pašalintume į dujas panašų monosilaną SiH 4 . Monosilanas išvalomas rektifikacijos, sorbcijos ir kitais metodais, po to dedamas ant silicio ir vandens, kurio temperatūra yra apie 1000 °C.
- Silicio valymas pramoniniu mastu atliekamas ne tarpinio silicio chlorinimo būdu. Taip ištirpsta sandėlio SiCl 4, SiHCl 3 ir SiH 2 Cl 2 puslankstės. Їх kitokiu būdu išvalykite namą (paprastai distiliavimo ir disproporcijos būdu) ir paskutiniame etape įpilkite gryno vandens, kurio temperatūra yra nuo 900 iki 1100 °C.
- Kuriamos pigesnės, švaresnės ir efektyvesnės pramoninės silicio valymo technologijos. Už 2010 metus prieš juos galima diegti silicio gryninimo vikariniu fluoru technologijas (pakeičiant chlorą); technologijos, kuriomis distiliavimas perkeliamas į silicio monoksidą; technologijos, pagrįstos vitražiniais namais, orientuotais į tarpkristalines ribas.
Vmіst domіshok ties galutiniu siliciu gali būti sumažintas iki 10 -8 -10 -6% masės. Daugiau pranešimų apie gryno silicio mitybą apžvelgiama straipsnyje Polikristalinis silicis.
Silicio gavimo gryno suskaidymo būdu metodas, kurį sukūrė Mikola, Mikolajovičius Beketovas.
Fizinė galia
Silicio kristalinė gardelė yra į kubinį paviršių kaip deimantas, parametras a = 0,54307 nm (esant aukštas spaustukas pašalinti kitas polimorfines silicio modifikacijas), bet per didesnį Si-Si atomų ryšį jungtimi su ryšiu zv'azku S-S silicio kietumas yra žymiai mažesnis nei deimanto. Silicio traškėjimas, tik kaitinamas 800 °C temperatūroje, tampa plastiška kalba. Vіn prozory už infrachervonogo viprominyuvannya s dozhini khvili 1,1 mikrono. Nosies drėgna koncentracija įkrovoje yra 5,81 10 15 m-3 (300 K temperatūrai).
Elektrofizinė galia
Elementarus silicis vieno kristalo pavidalu yra netiesioginio tarpo laidininkas. Aptvertos teritorijos plotis ties kambario temperatūra saugykla 1,12 eV, o esant T \u003d 0 K - 1,21 eV. Šlapių krūvininkų koncentracija silicyje normaliam protui tampa artima 1,5·10 10 cm −3 .
Dėl kristalinio silicio elektrotrofinės galios didžiulis antplūdis stato namus, kurie klaidžioja tamsoje. Norėdami išgauti gilaus laidumo silicio kristalus, į silicį įdėkite III grupės elementų atomus, tokius kaip boras, aliuminis, galis ir indis. Norėdami išgauti elektroninio laidumo silicio kristalus į silicį, įveskite atomus elementai V-ї groupi, pvz., fosforas, mish'yak, surma.
Kai elektroniniai prietaisai surenkami silicio pagrindu, svarbu prie medžiagos pritvirtinti paviršinį rutulį (iki dešimčių mikronų), todėl prie silicio elektrostatinės galios galima pridėti kristalo paviršiaus kokybę ir, matyt, apie gatavo įrankio galią. Sumontuojant tam tikrus įrenginius, pridedama vikrozė, taikoma modifikuojant paviršių, pavyzdžiui, paviršius padengiamas siliciu su įvairiomis cheminėmis medžiagomis ir її oprominennya.
Cheminė galia
Panašiai kaip anglies atomai, silicio atomai pasižymi orbitų sp 3 -hibridizacija. Ryšyje su hibridizacija iš gryno kristalinio silicio susidaro į deimantą panašūs grūdeliai, kuriuose silicis yra chotivalentinis. Tuo pačiu metu silicio garsas taip pat pasireiškia kaip chotivalentinis elementas, kurio oksidacijos būsena yra +4 arba -4. Zustrichayutsya dvivalentis pusiau silicis, pavyzdžiui, silicio oksidas (II) - SiO.
Normaliam protui silicis yra chemiškai neaktyvus ir aktyviai reaguoja tik su į dujas panašiu fluoru, kuriame ištirpsta lakusis silicio tetrafluoridas SiF4. Tokį silicio „neaktyvumą“ lemia nanodydžio silicio dioksido rutulio paviršiaus pasivavimas, kuris neigiamai nusėda esant rūgščiam, vėl ir vėl vandeniui (vandens garams).
parūgštinus ištirpusiu SiO 2 dioksidu, procesą lydi dioksido kamuoliuko tūrio padidėjimas paviršiuje, oksidacijos proceso stabilumą riboja atominės rūgšties ir kriokonservavimo dioksido difuzija.
Kaitinamas iki aukštesnės nei 400–500 °C temperatūros, silicis reaguoja su chloru, bromu ir jodu – sulankstytame sandėlyje įsisavinami lengvai lakūs tetrahalogenidai SiHal 4 ir, galbūt, halogenidai.
Su vandeniu silicis be vidurio nereaguoja, bet su vandeniu siliciu - silanai, kurių formulė Si n H 2n + 2 - turi netiesioginį būdą. Monosilane SiH 4 (jogas dažnai vadinamas tiesiog silanu) pastebimas metalų silicidų sąveikoje su rūgštimis, pavyzdžiui:
C a 2 S i + 4 H C l → 2 C a C l 2 + S i H 4 (\displaystyle ~(\mathsf (Ca_(2)Si+4HCl\ \rightarrow \ 2CaCl_(2)+SiH_(4)\ ) strėlė)))SiH 4 silanas, kuris ištirpsta šioje reakcijoje, keršija namus ir kitus silanus, zokremą, Si 2 H 6 disilaną ir Si 3 H 8 trisilaną, kai kuriuose silicio atomų lancetuose, sujungtuose viengubomis jungtimis (- Si -Si-Si- ).
Silicis reaguoja su azotu ir boru esant artimai 1000 °C temperatūrai, ištirpdydamas nitridą Si 3 N 4 ir termiškai bei chemiškai stabilų boridą SiB 3 , SiB 6 ir SiB 12 .
Esant aukštesnei nei 1000 ° C temperatūrai, galima naudoti silicį, kuris yra artimiausias periodinės lentelės analogas - anglis - silicio karbidas SiC (karborundas), kuris pasižymi dideliu kietumu ir mažu cheminiu aktyvumu. Karborundas plačiai naudojamas kaip abrazyvinė medžiaga. Tačiau dėl to silicio lydymas (1415 °C) tris valandas gali būti kontaktuojamas su akmens anglimi, atsižvelgiant į didelius izostatinio presavimo sukepinto smulkiagrūdžio grafito gabalėlius, kurie praktiškai nesikeičia ir netrukdo likusiam.
Apatiniai 4 grupės elementai (Ge, Sn, Pb) yra nepadengti siliciu, kaip ir dauguma kitų metalų. Kaitinant su siliciu ir metalais, gali susidaryti jų pusapvalkalai, silicidai. Silicidus galima suskirstyti į dvi grupes: joninius-kovalentinius (pudrų, balų-žemės metalų ir magnio tipo Ca 2 Si, Mg 2 Si ir in) ir metalinius (pereinamųjų metalų silicidai). Aktyvių metalų silicidai išdėliojami praskiedžiant rūgštis; Į metalus panašūs silicidai turi aukštą lydymosi temperatūrą (iki 2000 °C). Dažniausiai naudojami į metalą panašūs silicido sandėliai Aš Si, Aš 3Si2, Aš 2 Si 3, Aš 5 Si 3 i Aš Si 2. Į metalus panašūs silicidai yra chemiškai inertiški, atsparūs rūgštingumui aukštoje temperatūroje.
Ypač svarbu atkreipti dėmesį į tai, kad silicis užsandarina eutektinę sumą, leidžiančią sulydyti medžiagas, skirtas ferosilicio keramikos sandarinimui, esant temperatūrai, kuri yra pastebimai žemesnė, žemesnė nei sandariklio ir silicio lydymosi temperatūra.
Pridedant SiO 2 į silicį aukštesnėje nei 1200 ° C temperatūroje, silicio oksidas (II) - SiO ištirpsta. Šį procesą nuolat palaiko kristalų gamyba silicio metodais
Silicis vizijų priešakyje 1811 m. J.Gay-Lussac ir L.Tenaras, leidžiant silicio fluorido garus virš kalio metalo, baltymai nėra apibūdinami kaip elementas. Švedų chemikas J. Berzelius 1823 m kuriame aprašomas jo pašalintas silicis apdorojant kalio druską K 2 SiF 6 metaliniu kaliu aukštoje temperatūroje. Naujasis elementas buvo pavadintas „silicium“ (lot. silex – titnagas). Rusišką pavadinimą „silicis“ 1834 metais įvedė rusų chemikas Hermanas Ivanovičius Hessas. Išvertus iš kitos graikų kalbos. krhmnoz- Kut, kalne.
Žinios gamtoje, otrimannya:
Gamtoje silicis randamas vibruojančiame dioksiduose ir silikatuose kitame sandėlyje. Natūralus silicio dioksidas svarbesnis kvarco pavidalu, norint panaudoti kitus mineralus – kristobalitą, tridimitą, banginį, kusitą. Amorfinis silicio dioksidas kaupiasi diatominėse nuosėdose jūrų ir vandenynų dugne – šios nuosėdos nusėdo su SiO 2, patenkančios į diatomų ir kitų blakstienų sandėlį.
Vilniy silicis gali būti naudojamas skrudinimui su magnio traškiu baltu pisku, kuris chemijos sandėliui gali būti valomas silicio oksidu SiO 2 + 2Mg = 2MgO + Si. Pramonėje silicio techninis grynumas gaunamas lydant SiO 2 su koksu maždaug 1800 ° C temperatūroje lankinėse krosnyse. Tokio rango silicio grynumas gali siekti 99,9% (pagrindiniai namai yra anglis, metalas).
Fizinės galios:
Amorfinis silicis gali atrodyti kaip rudi milteliai, kurių tankis yra 2,0 g / cm3. Kristalinis silicis – tamsiai pilka, žvilganti kristalinė kalba, susikristalizavusi ir kieta, kristalizuojasi deimantuose. Tai tipinis laidininkas (geriau praleidžia elektrą, žemesnis izoliatoriaus tipo guminis, o aukštesnis laidininkui - vidurinis). Silicio traškėjimas, tik kaitinamas 800 °C temperatūroje, tampa plastiška kalba. Cіkavo, mokyklų mainai silicio prosorium į infrachervony viprominyuvannya, pradedant nuo ilgo vėjo 1,1 mikrono.
Cheminė galia:
Chemiškai mažai aktyvus silicis. Kambario temperatūroje reaguoja tik su į dujas panašiu fluoru, lakusis silicio tetrafluoridas SiF 4 šioje temperatūroje ištirpsta. Kaitinamas iki 400-500 °C temperatūros, silicis reaguoja su rūgštimi su ištirpusiu dioksidu, su chloru, bromu ir jodu - su ištirpusiais lengvai lakiais tetrahalogenidais SiHal 4 . Esant temperatūrai, artimai 1000 ° C, silicis reaguoja su azotu, kad ištirptų nitridą Si 3 N 4 su boru - termiškai ir chemiškai stabiliu boridu SiB 3, SiB 6 ir SiB 12. Su vandeniu silicis nereaguoja be tarpininkų.
Odinant siliciu, plačiausiai naudojama vandenilio fluorido ir azoto rūgščių suma.
Įkurti prie pievų.
Siliciui būdinga +4 arba -4 oksidacijos pakopa.
Svarbiausios sritys:
Silicio dioksidas, SiO 2- (Silicio anhidridas) ...
...
Silicio rūgštys- silpnas, neryškus, utvoryuyutsya, kai pridedant rūgšties į silikato dydį atrodo kaip gelis (želatinos kalba). Yra žinoma, kad H 4 SiO 4 (ortosilicis) ir H 2 SiO 3 (meta silicis arba silicis) skiriasi ir neatšaukiamai virsta SiO 2 kaitinant ir džiovinant. Kietas porėtas produktas, skirtas įvesti - silikagelis gali būti atidarytas ant paviršiaus ir kaip dujų adsorbentas, džiovinimo agentas, katalizatorius ir dilimo katalizatorius.
silikatas- gerųjų silicio rūgščių druskos (kriminiai natrio ir kalio silikatai) netirpsta vandenyje. galia.
Kriokliai- angliavandenių analogai, silani, pusiau nuoširdžiai, kai kuriuose silicio atomuose su viena jungtimi, jėga yakscho atomas silicio z'єdnаnі podvіyny zv'yazkom. Lances ir kiltsya naudojami panašiai kaip angliavandeniai. Visos galios gali dirbti savarankiškai, kartoti sumištus ir lengvai reaguoti su vandeniu.
Zastosuvannya:
Reikšmingiausias silicio kiekis žinomas renkantis lydinius aliuminio, vario ir magnio panaudojimui bei ferosilicidams, kurie gali būti svarbūs renkantis plieną ir šildymo įrangą. Silicio kristalai zastosovuyut sony baterijos ir napіvprovіdnikovih ūkiniai pastatai - tranzistoriai ir diodai. Silicis taip pat naudojamas kaip sirovinas gaminant organines silicio plokštes arba siloksanus, dažant aliejumi, aliejumi, plastikais ir sintetiniais kaučiukais. Neorganiniai šliužai Silicio vikoristas naudojamas keramikos ir plieno technologijose, kaip izoliacinė medžiaga ir p'ezokristalai
Kai kuriems organizmams silicis yra svarbus biogeninis elementas. Vіn įeikite į atraminių namelių sandėlį prie roslino ir skeleto - prie būtybių. Jūros organizmai – diatomės, dumbliai, radiolarijos, kempinės – susitelkę dideliuose silicio plotuose. Puikūs skaičiai asiūklių ir javų koncentratas su siliciu, pirmajame juodajame - bambuką ir ryžius primenantys pidrodinai, tarp jų - sodinami ryžiai. M'yazova audinys asmens keršyti (1-2) 10 -2% silicio, kaulinis audinys - 17 10 -4%, kraujas - 3,9 mg / l. Tačiau šiandien į žmogaus organizmą gali patekti iki 1 g silicio.
Antonovas S.M., Tomilinas K.G.
HF Tiumenės valstybinis universitetas, 571 grupė.
