Yüksek silikon konsantrasyonu. Nasıl biliyorsun
İşlemci? Pisok mu? Ve kelime çağrışımlarıyla ilgili ne var? Ya da belki Silikon Vadisi?
Sanki orada değilmiş gibi, bugün silikonla yapıştırıyoruz ve Si nedir ve neden yiyorsunuz diye bilmeniz gerekiyorsa, bir kedi istiyorum.
giriş
"Nanomalzemeler" uzmanlığında Moskova üniversitelerinden birinin öğrencisi olarak, sizi gezegenimizin en önemli kimyasal elementleriyle tanımak istiyorum sevgili okuyucu. Uzun zamandır bir şey seçiyorum, kömür veya silikon ve yine de Si'yi kendim kullanmaya karar verdim, böylece herhangi bir modern aygıtın kalbi ona dayanıyor, bu yüzden çok görkemli diyebilirsiniz. Düşüncelerimi son derece basit ve erişilebilir hale getirmeye çalışacağım, bu materyali yazdıktan sonra, onu özellikle yeni başlayanlar için kaydettim, ancak giderek daha fazla insan onu ağustos böceklerinden çıkarabiliyor, bu yüzden makalenin şunu söylemek istiyorum ilgi alanlarını genişletmek için özel olarak yazılmıştır, scho. Öyleyse başlayalım.
silisyum
Silikon (lat. Silisyum), Si, Mendeliev periyodik sisteminin IV grubunun kimyasal elementi; atomik numara 14, atom ağırlığı 28.086.
Doğada element üç kararlı izotopla temsil edilir: 28Si (%92,27), 29Si (%4,68) ve 30Si (%3,05).
Kalınlık (n.s.) 2,33 g/cm?
Erime noktası 1688 K

Toz Si
Tarihsel kanıt
Silikon tepeler, geniş topraklar, taş devrinden kalma bulvarlar. Binlerce çaça taşı ve taşın sulanması vardı. Zastosuvannya spoluk Silicon, işlenmesiyle bağlantılı - bir deponun hazırlanması - MÖ 3000 civarında başladı. e.(Eski Mısır). Evde daha önce silikon kullanıldı - oksit SiO2 (silika). 18. yüzyılda silika basit bir gövdeye enjekte edilerek (adında da geçen) “topraklara” taşınmıştır. І'yi kuran bir silika deposuna Skladnіst. I. Berzelius. Aynı vpershe'de, 1825'te, temel silikonu silisyum florür SiF4'ten çıkararak kalan metal potasyumun yerini aldı. Yeni elemente "silikyum" (Lat. silex - çakmaktaşı) adı verildi. Rus adı vvіv G. I. Hess, 1834 Roci'de.

Sonik sesin deposunda doğadaki uzantıların silikon yayı
Doğada genişleyen silikon
Yerkabuğundaki genişlik için Silikon başka bir (ekşiden sonra) elementtir, litosferdeki ortalaması% 29,5'tir (kütlenin arkasında). Dünyanın kabuğu Silikon grisi, yaratığın dünyevi dünyasının kömürü gibi aynı birincil role sahiptir. Silikonun jeokimyası için, özellikle yogo ve ekşi arasındaki bağlantı önemlidir. Litosferin %12'ye yakın bir kısmı kuvars minerali ve çeşitli çeşitleri şeklinde silis SiO2 haline gelir. Litosferin %75'i çeşitli silikatlardan ve alüminosilikatlardan (polova, mika, amfibol toshcho) oluşur. Silika ile yer değiştirebilen toplam mineral sayısı 400'ü geçmektedir.
Silikonun fiziksel gücü
Bence özellikle varto değil, hepsi bu Fiziksel güçÜcretsiz erişimim var, ancak en yaygın olanları listeleyeceğim.
Kaynama noktası 2600 °C
Dovgokhvilovyh ІCh-promenіv için silikon prozorium
Dielektrik penetrasyon 11.7
Mohs Silikon Sertliği 7.0
Silikon eğilimli malzemenin, hatıra plastik deformasyonunun 800°C'nin üzerindeki sıcaklıklarda başladığını söylemek isterim.
Silikon bir iletkendir, pek çok zastosuvannya bildiğimiz şarapla aynıdır. Silikonun elektrik gücü evin içinde olabilir.
Kimyasal güç.
Burası zengin, harika diyebilir ama ben en ünlüsüne rastlıyorum. Raflarda Si (karbona benzer) 4 değerlikli.
Silisyum zavdyak yüzeyinde oksit eritme, yüksek sıcaklıklarda rüzgara karşı kararlıdır. Asit içinde 400 °C'de oksitlenerek silikon oksit (IV) SiO2'yi çözer.
Silikon asitlere karşı dayanıklıdır ve nitrik ve hidroflorik asitlerle karışma olasılığı daha düşüktür, sıcak çayırlarda su görmeden kolayca ayırt edilir.
Silikon, 2 grup asidik silan yapar - siloksan ve siloksenyum. Silikon, 1000 °C'nin üzerindeki sıcaklıklarda nitrojen ile reaksiyona girer. kimya endüstrisi için olduğu kadar yangın söndürücü üretimi için de değerli bir malzemedir. Termal ve kimyasal direncin yanı sıra yüksek sertlik, silisyum karbür (silikon karbür SiC) ve boron (SiB3, SiB6, SiB12) zeminlerle işlenir.
Otrimanya Silikon
Bence tse naytsіkavіsha kısmı, işte rapor.
Nadas tanıma türü ayrılır:
1.
silikon elektronik güç(t.z. elektronik silikon") - Taşıyıcı için Kombolniy Iz Vmist Kluman Puna'nın NUBILSH'si 99.999 %, Elektrikli Opir Elekniye Yytno'nun Petomy'si, izhntervili'de yaklaşık 0.001 ila 150 ohm cm arasında paçavra olabilirim, Ale suçlu ev, ilgilenmek istiyor elektrik opirinin kreş görevlerinin, çınlaması, kabul edilemez.
2.
silikon sony kalitesi(t.z. "sonyachny silikon") - fotoelektrik dönüştürme cihazlarının (sonik piller) üretiminde kullanılan, fiber başına% 99,99'un üzerinde karışık silikondan silikon.

3.
teknik silikon- saftan karbotermik yenileme yöntemiyle alınan silikon polikristal yapı blokları kuvars gıcırtı; % 98 silikon ile kaplayın, ana ev kömürdür, yüksek miktarda hafif elementlerle havalandırılır - bor, fosfor, alüminyum; çoğunlukla dolaylı olarak polikristalin silikon bulundurmak için kullanılır.
Teknik saflıkta silikon (%95-98), grafit elektrotlar arasında esinli silis SiO2 elektrik patlamalarına sahiptir. Saf ve özellikle saf silikon elde etmek için nap_v_dnikovoї tehnіko razrobleno yönteminin geliştirilmesi ile bağlantılı olarak. Saf vih_dnih spoluk silikonun ileri sentezi uğruna, z yakikh vityagyat silіkі vіdnovlennya vіdnovlennya аbo termіchnogo razkladannya.
Polikristalin silikon ("polisilikon") - ticari olarak uygun silikonun en saf formu, - teknik silikonun klorür ve florür yöntemleriyle saflaştırılması için kullanılan ve mono- ve multi-kristalin üretiminde galip gelen bir ürün silikon.
Geleneksel olarak, polikristalin silikon, teknik silikondan, yogayı silan musluklarına (monosilan, klorosilan, florosilan) transfer etme yolu ile çıkarılır. .
Saf silikon iletkenler iki tipte elde edilir: çok kristalli(SiCl4 veya SiHCl3'ün çinko veya su ile güçlendirilmesi, SiI4 ve SiH4'ün termal genleşmesi) ve monokristal(Potasız bölge erimesi ve tek bir kristalin erimiş silikondan "sarılması" - Czochralsky yöntemi).

Burada silikonu titreştirmek için Czochralski yöntemini kullanabilirsiniz.
Czochralski yöntemi- bir tohum kristali (veya çok sayıda kristal) getirme yolu ile bir kristalleşme koçanının başlatılmasıyla eritmek için büyük bir zorunluluk olan geniş bir yüzeyde bir dağda sarma yolu ile kristalleri titreştirme yöntemi eriyen bir yüzeyin üzerinde belirli bir yapı ve kristalografik temas.
Zastosuvannya Silikon
Özel alaşımlı silikon, elektrik iletkenlerinin (transistörler, termistörler, güç vibratörleri, tristörler; uzay gemilerinde kullanılan sony fotoselleri ve daha pek çok şey) hazırlanmasında yaygın olarak kullanılan bir malzemedir.
1 ila 9 mikron büyüklüğündeki uzun tüyleri değiştirmek için silikon prosoria parçaları, kızılötesi optiğe yerleştirilebilir.
Silikon farklı olabilir ve genişleyen zastosuvannya'nın tüm alanları. Metalurjide Si
erimiş metallerden ekşiliğin (deoksidasyon) giderilmesi için vikoristovuetsya.
Silikon depo salon ve renkli metallerin çok sayıda alaşımı.
Korozyona karşı direnci artırmak, livar güçlerini iyileştirmek ve mekanik dayanımı artırmak için sağlam Silikon alaşımları; daha büyük bir zmistі ile prote Silikon kryhkіst viklikati yapabilir.
En önemlileri, kayışların intikamını almak için kullanılabilecek alaşımlar, bakır ve alüminyum alaşımlarıdır.
Silika, cam, çimento, seramik, elektrikli ve diğer endüstriyel gazlı bezlerle işlenir.
Silikon temizliği, tek elektronik cihazların (örneğin, bilgisayarınızın işlemcisi) ve tek çipli mikro devrelerin üretimi için önemlidir.
Saf silikon için kullanılan saf silikon, metalurjik silikonun kristal silikon olarak saflaştırılması, sony enerji için ana hammaddedir.
Tek kristalli silikon - elektronik ve sony güç mühendisliğinin kreması, gaz lazerlerinin aynalarını yapmak için kullanılır.

Temizleme silikonu ve yoga ürünü
Vücuttaki silikon
Vücuttaki silikon, sert iskelet parçalarının ve dokuların aydınlatılmasında baş sıralarda yer alan çeşitli spolukların gözlerinde bulunur. Özellikle silikon açısından zengin olan deniz yosunu (örneğin, iki atomlu algler) ve canlılar (örneğin, silikon boynuzlu süngerler, radyolarya) okyanusun dibindeki okyanusun dibindeki silikon oksit birikintileriyle sertleşen canlıları (örneğin, silikon boynuzlu süngerler, radyolarya) biriktirebilir. (IV). Soğuk denizlerde ve göllerde, silikon açısından zengin biyojenik katırlar, tropikal denizlerde - düşük silikon içeriğine sahip vaping katırları - daha önemlidir. Otlar, sazlar, palmiye ağaçları ve at kuyruğu, karasal büyümenin ortasında çok fazla silikon biriktirir. Omurga canlılarında silisyum (IV) oksit yerine, kül nehirlerinde %0,1-0,5 oranında. Alkalideki en fazla sayıda silikon tezahüründe mutlu kumaş, nirkah, pidshlunkovy kasası. Ek bir diyette, insanlar 1 g'a kadar silikona sahiptir. Havadaki yüksek silikon (IV) oksit alımı ile, hastalığa neden olan bir kişinin legenia'sında tüketilir - silikoz.
Visnovok
Peki, her şeyden, sonuna kadar okuduysanız ve biraz nüfuz ettiyseniz, o zaman başarıya biraz daha yakınsınız demektir. Spodіvayus, boşuna yazmadım ve hoch komu'ya kefil oldum. saygı için.
SİLİKON. (Silikyum), Si - kimya. periyodik element sistemi grubunun IV. elementi; at. N. 14, at. m.28.086. Reçinemsi parlaklığa sahip kristalin silikon-koyu gri konuşma. Çoğu durumda, oksidasyon derecesi ortaya çıkar - 4, +2 ve +4. Doğal silikon, 28Si (%92,28), 29Si (%4,67) ve 30Si (%3,05) kararlı izotoplarından oluşur. Radyoaktif izotoplar 27Si, 31Si ve 32Si'nin 4,5 saniye, 2,62 yıl ve 700 yıl ters bozunma periyotlarıyla çekilmesi. ilk olarak 1811'de görüldü Fransızca. kimyager ve fizikçi J. L. Gay-Lussac ve French. kimyager LJ Tenar, ancak 1823'te daha az tanımlama var İsveçli, kimyager ve mineralog J. Ya. Berzelius.
Yerkabuğundaki genişlik için (%27,6), silisyum-diğer (ekşiden sonra) element. Bilmek önemlidir. silika Si02 ve diğer ekşi konuşmalar (silikatlar, alüminosilikatlar, vb.) şeklinde. En iyi beyinler için, periyodu a = 5,4307 A olan, elmas gibi yüz merkezli kübik bir yapıya sahip kararlı bir peçete modifikasyonu kurulur. Aralıklı penetrasyon 2,35 A'dır. Genişlik 2,328 gcm'dir. Yüksek basınçla (120-150 kbar) daha büyük kablolara ve metal modifikasyonlara geçin. 6.7 K geçiş sıcaklığına sahip metal modifikasyonu süper iletken. Artan basınçla, erime noktası 1 bar basınçta 1415 ± 3 ° C'den 15.104 bar basınçta 810 ° C'ye düşer (bir borunun ısınma kaybı noktası) , metal katran). ). Eridiğinde, atomlar arası bağların koordinasyon sayısında ve metalleşmesinde bir artış olur. Kısa menzilli düzenin amorf silisik karakteri, güçlü bir şekilde oluşturulmuş hacim merkezli kübik bir yapı gösterir, nadire yakındır. Debievskaya t-ra, 645 K. Coef'e yakındır. sıcaklık lineer genleşmesi, aşırı yasaya göre değişen t-ri ile değişir, t-ri 100'den düşük Şarap için, t-ri 80 K'de minimum (-0,77 10 -6) derece -1'e ulaşarak negatif olur; t-rі 310 K şarapta 2.33 10-6 derece-1 ve t-rі 1273 K-4.8 10 derece-1'dir. Erime ısısı 11.9 kcal/g-atom; tkіp.3520 K.
Erime sıcaklığında süblimleşme ve buharlaşma ısısı 110 ve 98.1 kcal/g-atomdur. Silisyumun termal iletkenliği ve elektriksel iletkenliği, kristallerin saflığında ve kusursuzluğunda yatmaktadır. Zі rostannyam t-ri coef. saf K.'nin termal iletkenliği kademeli olarak artar (t-ri 35 K'de 8.4 cal/cm X X sn dereceye kadar) ve sonra değişir, t-ri vіdpovidno 300 ve 1200 K'de 0.36 ve 0.06 cal/cm sn dereceye ulaşır. Entalpi, entropi ve ısı kapasitesi K. standart zihinlerde, 770 cal/g-atom, 4.51 ve 4.83 cal/g-atom - dereceye eşittir. Silikon diyamanyetik, katı (-1,1 10 -7 mu/g) ve nadir (-0,8 10 -7 mu/g) manyetik duyarlılığı. Silikon, t-ri'de zayıf bir şekilde biriktirilir. Nadir K.'nin erime sıcaklığında yüzey enerjisi, kalınlığı ve kinematik viskozitesi 737 erg/cm2, 2.55 g/cm3 ve 3 10 m2/sn olur. t-p 0'da 1,08 u - t-p 300 K'de 1,15 ev çitle çevrili bölge genişliğine sahip tipik bir kristal silikon iletken. Oda sıcaklığında, ıslak taşıma yüklerinin konsantrasyonu 1,4 · 10 · 10 cm - 3'e yakındır;
Silisyumun düşme gücü, evlerin doğası ve konsantrasyonunun yanı sıra kristalin mükemmelliğinden kaynaklanmaktadır. Otrimannya napіvprovіdnikovogo Do için yüzük. p- ve n-tipi yoga iletimi ile, suyun alıcıya geçişini oluşturan IIIb (bor, alüminyum, galyum) ve Vb (fosfor, miş'yak, antimon, bizmut) alt grubu elementleri ile birleştirilirler. ve kortekse yakın donör bölgeleri, rostash Vikoristin alaşımlanması için, diğer elementler (örneğin) bu şekilde şekillendirilir. glybokі rivnі, yakі obumovlyuyut burnsіїv suçlamalarının gömülmesi ve rekombinasyonu. Tse, yüksek elektro ile malzeme almanızı sağlar. farklı müştemilat sayısındaki artış için önemli olan küçük aşınma yüklerinin tabanının küçük önemsizliğini destekleyin (t-rі 80 K'da 1010 ohm cm). katsayı silikonlu termoelektrik güç sadece t-ri'de ve evin yerine biriktirilecek, zbіlshyuyuchi zі zrostannym elektroopor (p = 0.6 ohm - cm, a = 103 mikrovolt / dolu). Silikonun dielektrik penetrasyonu (11 ila 15 arası) depoda ve monokristallerin bütünlüğünde zayıf bir şekilde biriktirilir. Silikonun optik killenmesi yasaları, saflık, konsantrasyon ve yaşamdaki kusurların doğası ve ayrıca uzun ömür nedeniyle büyük ölçüde değişir.
Elektromanyetik kolivan dolaylı killeme kordonu 1,09 avroya yakın, doğrudan killeme - 3,3 avroya kadar. Karmaşık kırılma göstergesinin (nik - ik) parametrelerinin spektrumunun görünür bölgesinde, evin yüzeyinde yatmak zaten mümkündür. Özellikle saf Do için. (deλ \u003d 5461 A ve t-re 293 K) n \u003d 4.056 ve k \u003d 0.028. Elektroniğin robot çıktısı 48 avroya yakın. Silikon trendi. Moos - 7 için Yogo sertliği (t-ra 300 K); YB = 240; HV y \u003d 103; ben = 1250 kgf/mm2; norm modülü, esneklik (polikristal) 10890 kgf/mm2. Mineralite arasında kristalin derinliğinde yatın: viginde, derinlik 7 ila 14'tür; katsayı Sertlik 0,325 1066 cm2/kg.
Oda sıcaklığında, silikon pratik olarak gaz benzeri (dahil) ve katı reaktiflerle etkileşime girmez, krіm lіv. t-ri'yi hareket ettirirken, metaller ve metal olmayanlar ile aktif bir etkileşim vardır. SiC karbürü (sıcaklık 1600 K'de), Si3N4 nitrürü (sıcaklık 1300 K'de), fosfit SiP'yi (sıcaklık 1200 K'de) ve arsenit Si As, SiAS2'yi (sıcaklık 1000 K'de) çözen Zocrema. 700 K sıcaklıkta ekşi reaksiyonla, Si02 dioksitin halojenlerle söndürülmesi - SiF4 florür (300 K'den yüksek bir sıcaklıkta), SiCl4 klorür (500 K'den yüksek bir sıcaklıkta), SiBr4 bromür (bir sıcaklıkta) 700 K) ve SiI4 düğümü (en 1000'de). Diğerleriyle yoğun bir şekilde tepki veriyor. ki kimya yerine ikamelerinde katı farklılıklar oluşturan metaller. yarı - silisitler. Katı güllerin homojenlik alanları, rozetin doğasına bağlı olarak oluşur (örneğin, Nimechchin'de %0 ila 100, sonbaharda %15'e kadar, alfa zirkonyumda %0,1'den az).
Katı silikondaki metaller ve metal olmayanlar arasındaki fark önemli ölçüde daha azdır ve kulağa retrograd gelir. Ne sınırları olan, bir ev yerine, ne yapılıyor. çok derin değil, maksimuma ulaşın ( 2 10 18 , 10 19 , 2 10 19 , 1021, 2 10 21 cm) alan t-r 1400 ila 1600 K arasında. Derin rіvenny vіdznyayutsya ile evler biraz daha küçük rozchinnіstyu (selenyum için 1015 ve nikel için 7 10 17'ye kadar zalіza için 5 10 16 ve midi için 10 18 cm-3). Nadir bir çelikte silikon, genellikle büyük ısı vizyonları olan sıradan metallerle çevrili değildir. Saf silikon, elektrikli fırınlarda kuvars ve kömür ile temperlenmiş %99 Si і - %0.03 Fe, Al і Co teknik bir üründen hazırlanır. Yeni bir nefesle oralara (sum_shy hidroklorik ve sirchanoy ve ardından florür-su ve sirchanoy) evlere başlanır, bundan sonra ürün (%99,98) alınır, klor ile muamele edilir. Sentezler damıtma ile saflaştırılır.
Silikon iletken, SiCl4 klorür (veya SiHCl3) ile birlikte suda veya SiH4 hidritin termal genleşmesinde kullanılır. Monokristallerin artık saflaştırılması ve öğütülmesi, özellikle saf sos (1010-1013 cm-3'e kadar evde) cf\u003e 10 3 ohm cm dozlama dikkate alınarak, potasız bölge pürüzsüz yöntemiyle veya Czochralsky yöntemiyle gerçekleştirilir. Gerekli evlerin sayısı. 2-4 çapında ve 3-10 cm uzunluğunda silindirik kremleri bu şekilde hazırlarsınız.Özel için. amaç daha fazla monokristal üretmektir. Asitli çelikler ve alaşımlar gibi asitli tuzlu sudan teknik silikon ve özellikle yogo alaşımları ve ayrıca hafif katkı maddeleri. Özellikle çeşitli elementlerle katkılanmış saf zrazki tek kristal K.'nin çeşitli düşük akımlı (zocrema, termoelektrik, radyo, ışık ve fototeknik) ve yüksek akımlı (titreşimli, dönüştürücü) bağlantıların temeli olarak kullanıldığı bilinmektedir.
Silisyum ve silikon
Silisyum metal olmayan hale getirilir ve 4 elektron aynı enerji seviyesinde olabilir. Vіn, oksidasyon aşaması + 4'ü gösteren vіddavati їх olabilir ve oksidasyon aşaması - 4'ü gösteren elektronlar ekleyebilir. Bununla birlikte, silikona elektron ekleme yeteneği önemli ölçüde daha azdır, karbona göre daha düşüktür. Silikon atomları daha büyük bir yarıçapa, daha düşük karbon atomlarına sahip olabilir.
Doğanın silikon bilgisi .
Doğadaki uzantıların silikon kemeri. kütlenin% 26'sının üzerindeki düşüşün її kısmı başına kızamık. Şarapların eni için başka bir yere (ekşiden sonra) oturtun. Vіdmіnu'da uglec C vіlny stіnі vіrіdі zustrichaetsya değil. Depoya çeşitli kimyasal bileşimler, esas olarak çeşitli silikon oksit (IV) modifikasyonları ve silisik asit tuzları (silikatlar) girer.
silikon takıntısı .
Teknik saflıkta (%95 - 98) endüstriyel sınıf silikon, SiO ağırlıklıdır 2 Kavurma sırasında elektrikli fırınlarda kola:
SiO 2 + 2C \u003d Si + 2CO
SiO 2 + 2Mg \u003d Si + 2MgO
Bu şekilde evlerden kahverengi renkli amorf silikon tozu alınır. Eriyen metallerden (Zn, Al) yeniden kristalleştirme, bir kristal değirmene aktarılabilir.
Yüksek saflıkta bile silikon tetraklorür, silikon tetraklorür SiCl için 1000°C'de kullanılır. 4 çift çinko:
SiCl4 + 2Zn \u003d Si + 2ZnCl2
özel yöntemlerle arındıran yogo.
Fiziksel Kimyasal güç silikon.
Saf kristal silikon - eğimli ve sert, gevşek eğim. Bir elmas gibi, kovalent tipte bir bağa sahip kübik bir kristal kafesi vardır. Yogo erime noktası 1423 °C. En büyük beyinler için, yalnızca flor ile reaksiyona giren, ancak ısıtıldığında çeşitli kimyasal reaksiyonlara giren aktif olmayan bir silikon elementi.
napіvprovіdnikovіy tehnіtsі için değerli bir malzeme olarak Yogo vikoristovuyut. Diğer şarap iletkenleriyle eşleştirildiğinde, seyreltik asitlere karşı önemli bir direnç ve 300 ° C'ye kadar büyük bir elektrik direnci ile ayırt edilir. Teknik silikon ve ferrosilikon ısıya dayanıklı, aside dayanıklı ve takım çelikleri, chavuns ve diğer zengin alaşımlar için metalurjide de yardımcıdır.
silikon metaller ile kimya, Silisitler olarak adlandırılır, magnezyum ile ısıtıldığında magnezyum silisit çözülür:
Si + 2Mg = Mg2Si
Bu hakimiyetin arkasındaki metal silisitler, karbürleri öngörür, bu nedenle metal benzeri silisitler, tıpkı metal benzeri karbürler gibi, büyük sertlik, yüksek erime noktası, sıcak elektrik iletkenliği ile ayırt edilir.
Sumish pisku'yu elektrikli fırınlarda kola ile kızartırken, silisyum karbür ve karbon, silisyum karbür veya karborundum ile karıştırılır:
SiO2 + 3C = SiC + 2CO
Carborundum, refrakter, barless sert konuşma, değerli bir aşındırıcı ve ısı malzemesidir. Carborundum, yak i, maє atomik kristal grati. Temiz istasyonda bir yalıtkan var ama evin varlığında iletken oluyor.
silikon yak ben , iki oksidi çözer: silikon oksit (II) SiO ve silikon oksit (IV) SiO 2 . Silikon oksit (IV), serbest ülkede doğası gereği geniş çapta genişleyen sert bir refrakter konuşmadır. Suda veya hidroflorik asitte yalnızca flor ve gaz benzeri flor ile etkileşime giren kimyasal olarak kararlı konuşma:
SiO 2 + 2F 2 \u003d SiF 4 + O 2
SiO2 + 4HF \u003d SiF4 + 2H20
Doğrudan reaksiyonlara işaret etmek, silikonun florine karşı büyük bir dağınıklığa sahip olabilmesi gerçeğiyle açıklanır. Ek olarak, silikon tetraflorür uçan bir konuşmadır.
tekhnіtsі prozoriya SiO'da 2 Kararlı bir refrakter kuvars levhanın hazırlanması için vykorovuyut, ultraviyole değişimini nazikçe özlediğinden, sıcaklıktaki önemli değişiklikleri gösteren büyük bir genleşme katsayısına sahip olabilir. Silikon oksit (II) tripoli maє büyük gözenekliliğin amorf modifikasyonu. Titreşimli dinamit (burun vibukhovo konuşması) vb. İçin bir ısı ve ses yalıtkanı olarak Yogo vikoristovuyut. Titreşimli bir seste silikon (IV) oksit ana etkenlerden biridir. günlük malzemeler. Ateşe ve aside dayanıklı malzemelerin üretiminde, çelikte, metalurjide bir eritken gibi, vb.
Moleküler formüllere göre, karbon oksit (IV) ve silikon oksitin (IV) kimyasal ve fiziksel güçlerinin eşleşmesi kolaydır, bunların gücü benzerdir. kimyasal depo z'ednan raznі. Neden silikon oksidin (IV) sadece SiO moleküllerinden oluşmadığı açıklanıyor? 2 s їх ortakları gibi, bazılarında silikon atomları ekşi atomları ile birleştirilir. Silikon (IV) oksit (SiO 2 )N. Meydandaki resim її:
D. I. Periyodik sisteminin IV grubunun baş alt grubunun (IVA grubu) elemanlarının bir başka temsilcisi. Mendeliev - silikon Si.
Doğada, asit genişliği için başka bir kimyasal element silikondur. Yerkabuğu, yogo spoluk'tan üç ayda bir giderek daha fazla katlanıyor. En yaygın silikon, silikon oksit (IV) SiO 2'dir, diğer adı silikadır. Doğada, şaraplar mineral kuvars (küçük 158), bu tür zengin bir çeşitlilik - girsky kristali ve ayrıca ünlü leylak formu - ametist ve ayrıca akik, opal, jasper, kalsedon, carnelian şeklinde yapılır. virobnі ve sarhoş edici taşlar. Silisyum (IV) oksit de dikkat çekici ve kuvars kumlarından oluşur.

Mal. 158.
Dolomit serpiştirilmiş kuvars kristalleri
Silikon oksit (IV) bazlı üç farklı mineral (çakmaktaşı, kalsedon ve diğerleri) ilk insanlar znaraddya pracі hazırladı. Göze çarpmayan ve bir taştan daha dar olmayan aynı çakmaktaşı, bir taş koçanını döşemek vіtsі - vіtsі kremіnyh znaryad pratsі (Şek. 159). Bunun iki sebebi vardır: çakmaktaşının genişliği ve bulunabilirliği ile binaların kenarlarının ne kadar keskin olduğu inşa edilmesi.

Mal. 159.
Znaryaddya taş vіku
Silikon için başka bir doğal malzeme türü silikattır. Bunlar arasında en büyük genişlikteki alüminosilikatlar vardır (bu silikatların alüminyum kimyasal elementin yerini alabileceği anlaşılmıştır). Alüminosilikatlara granit eklenir, farklı görmek kil, mika. Alüminyumun öcünü almayan silikat, örneğin havai fişek yapımında kullanılan asbest.
Silikon oksit (IV) SiO 2 yetiştiricilerin ve canlıların yaşamı için gereklidir. Şaraplar, yaratıkların roslin ve zahisnymi peçelerinin saplarını verir (Şek. 160). Size zavdyaks, sıralar, kuyruklar ve at kuyrukları, bagetler gibi mitzno, bıçaklar gibi kesilmiş gostre yapraklı sazlar, bir kafa gibi eğimli bir alanda anız ve mitzna hasırlarında mısır tarlalarının uzanmasına izin vermeyen tahıl sapları ormandaki tarlalar ve rüzgar. Luska kaburga, koma kabukları, krill meteliks, pir'ya ptahiv mіtsnі yaratıklarının yünü, oskіlki smite silika.

Mal. 160.
Silikon (IV) oksit, roslinin gövdelerine ve canlıların boğucu kıvrımlarına minerallik verir.
Z'ednannya silikon, bir kişinin saçına ve tırnaklarına pürüzsüzlük ve yumuşaklık verir.
Silikon, alt canlı organizmaların deposuna - diatomlar ve radyolaryalar, canlı maddenin en alt göğüsleri, sanki silika ile iskeletin güzelliğinin arkasında kusurlarını yaratıyormuş gibi (Şek. 161).
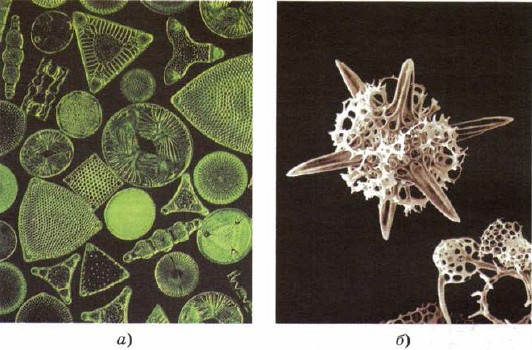
Mal. 161.
Diyatomların (a) ve radyolarların (b) iskeletleri silikadan oluşur
silikonun hakimiyeti. Sony pilli bir mikro hesap makinesi kullanıyorsunuz ve bu nedenle kristal silikonla ilgili bir bildirim var. Tse napіvprovіdnik. Vіdmіnu vіd metalіv üzerinde, pіdvishennyam sıcaklığı yogo elektroprovіdnіst zbіshuєtsya. Uydulara, uzay gemilerine, istasyonlara ve dahah budinkiv'e (küçük 162), sony enerjisini elektriğe dönüştüren sony pilleri takıyorlar. Pis koku, napіvprovіdnikіv kristalleri ve ilk siyah çakmaktaşı ile çalışır. Silikon fotoseller, killi sony enerjisinin %10'una kadar elektriğe dönüştürülebilir.

Mal. 162.
Dahu kabini için uykulu pil
Asitlikte yanan silikon, sizi tatmin eden silikon oksit (IV):
![]()
Metal olmayan silikon, ısıtıldığında metallerle silisit çözeltileriyle birleşir, örneğin:
![]()
Silisitler, gaz benzeri su benzeri bir silikon - silan gördüğünüzde su veya asitlerle kolayca yayılır:
Karbonhidratların yüzeyinde, yüzeydeki silan çözünmüş silikon oksit (IV) ve su ile kendiliğinden birleşir ve yanar:
Silan ve metan CH 4 arasındaki artan reaksiyon, silikon atomunun genleşmesinin daha büyük olması, karbonda daha düşük olması, dolayısıyla Si-H kimyasal bağlarının daha küçük, C-H bağlarının daha düşük olması ile açıklanır.
Çayırların konsantre su değişimleriyle silikon etkileşimi, silikat ve su oluşturma:
Silikon, silikon oksit (IV) magnezyum veya karbona benzer:
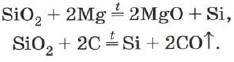
Silikon oksit (IV) veya silikon dioksit veya silika SiO 2 yak і CO 2 є asidik oksit. Bununla birlikte, CO2'nin yüzeyinde moleküler ama atomik bir kristal kafes vardır. Buna göre SiO 2 sert ve inatçı bir konuşmadır. Şaraplar, silisik asit - silikatların çözünmüş tuzları ile çayırlarda yüksek sıcaklıklarda su asitleri, hidroflorik krema ve aloe bakımından farklılık göstermez:
Silika, silikon oksidi (IV) metal oksitler veya karbonatlarla alaşımlamak için de kullanılabilir:
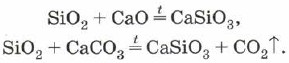
Sodyum silikatlar ve potasyum, perakende levhalar olarak adlandırılır. Їх su tedarik etmek- Silikat yapıştırıcı kullanmakta fayda var.
Silik asit H2Si03 (Şek. 163):
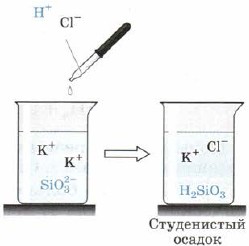
Mal. 163. Silikat iyonuna asit reaksiyonu
Ayrıca H2SiO3 de zayıf asittir. Suda tutarsızdır ve kuşatmanın tortusuna bakarken gerici kargaşadan düşer, bazen farkın tüm hacmini sıkıştırarak katı bir kütleye dönüştürür, pelteye, pelteye giderim. Masi asarken, oldukça gözenekli bir konuşma - diğer konuşmaların bir adsorban - kili olarak yaygın olarak kullanılan silika jel oluşturulur.
Laboratuvar Sertifikası No. 40
Silisik asit bulundurmak ve gücün doğrulanması
silikon enjeksiyonu. Silikonun hem iletken malzemelerin hem de aside dayanıklı alaşımların üretiminde kullanıldığını zaten biliyorsunuz. Kuvars kumu yüksek sıcaklıklarda yünle kaynaştığında, yalnızca elmasta bulunan silisyum karbür SiC çözülür. Bu nedenle, metalorіzalnyh verstatіv rіztsіv bileme ve pahalı taş parlatma için vicorate gereklidir.
Erimiş kuvarstan, yüksek sıcaklıklara dayanabilen ve soğukta çatlamayan çeşitli kimyasal kuvars kaplar hazırlanır.
Z'ednannya silikon є deponun çimentoya bükülmesinin temeli.
Zvichayne hatası, Na 2 O CaO 6SiO 2 formülü ile ifade edilebilen depo olabilir. Yogo, eritilmiş sumish soda, vapnyak ve piska ile özel fırınlarda kazanılır.
Vіdmіnna pirinç skla - zdatnіst rozm'yakshuvatisya і erimiş çelikte, depo yakalandığında kurtarıldığı için bir form olup olmadığı şişer. Gereçler ve diğer eşyalar temel alınarak yapılır.
Dodatkovі yakosti sklu farklı katkı maddeleri verir. Böylece, kurşun oksit girişi kristal berraklığında bir renge indirgenir, krom oksit yeşil renkli olur, kobalt oksit mavi olur vb. (Şek. 164).

Mal. 164.
Renk deposundan ürünler
Sklo, halkın en eski şarap üreticilerinden biridir. Zaten 3-4 porsuk. Bu nedenle Mısır, Suriye, Finiki ve Karadeniz'de savaş çıktı.
Sklo - aynı malzeme remіsnikіv'den daha az değil, aynı zamanda sanatçılar. Usta, en yüksek mükemmellik seviyesine ulaştı Antik Roma, sanki mozaiklerinin renk eğimini ve işçiliğini alıp götürebilmişler gibi.

Mal. 165.
Chartres, Notre Dame Katedrali'nin vitray pencerelerinde renkli cam
Harika bir müzenin obov'yazkovymi nitelikleri ve kilisenin renkli vitray pencereleri, mozaik paneller - bunun parlak izmaritleri ile depodan sanat eserleri yaratın (Şek. 165). Rusya Bilimler Akademisi'nin St. Petersburg şubesinin tesislerinden birinde, muzaffer M. V. Lomonosov olan Peter I'in mozaik bir portresi var (Şek. 166).

Mal. 166.
Peter I'in mozaik portresi
Tıkanıklık alanları oldukça geniştir. Tse vikonne, plyashkove, lampov, dzerkalne sklo; optik eğim - göz merceklerinden kamera gözlüklerine; ayırt edilemez optik cihazların lensleri - mikroskoplardan teleskoplara.
İkinci en önemli malzeme olan silikon esaslı kaplamalar ise çimentodur. Yogo, sarılmış özel fırınlarda kil ve vape pişirmek için kullanılır.
Çimento tozu su ile karıştırılırsa, çimento sağlam bir şekilde kurulmaz, aksi takdirde çalar saat olarak adlandırılan, adım adım daha sert olan çimento rozchin. Çimento veya mıcıra beton eklenirken son kat gibi beton çıkarılmalıdır. Betonun önemliliği artıyor, böylece yeni çerçeveye yeni bir çerçeve giriyor - panel duvarlarının, bindirme bloklarının, fermi köprülerin vb. Yapıldığı dökme beton çıkıyor.
Depo çimento üretimi yapmaktadır. silikat endüstrisi. Vaughn ayrıca silikat seramikler - ceglu, porselen (küçük 167), fayans ve bunlardan ürünler üretiyor.

Mal. 167.
porselen çeşitleri
Vіdkrittya silikon. Eski zamanlarda insanlar silisyum kullanımında geniş çapta muzaffer olsalar da, silisyumun kendisi ilk olarak 1824 yılında İsveçli kimyager J. Ya. Berzelius tarafından elinden alındı. Ancak 12 yıl önce yeni çakmaktaşı J. Gay-Lussac ve L. Tenard götürüldü, ale vin duzhe zabrudneniy evleri.
Latince adı silicum, koçanını Latince silex-çakmaktaşı kelimesinden alır. Rus adı "silikon" ceviz kremnos'a benziyor - "skel, skel".
Anlayan yeni kelimeler
- Doğal silikon kaynakları: silika, kuvars ve diğer çeşitler, silika, alüminosilikat, asbest.
- Silisyumun biyolojik önemi.
- Silikonun hakimiyeti: napіvprovіdnikovі, ekşi, metaller, çayırlar ile etkileşim.
- Silan.
- Silikon (IV) oksit. Yoga Budova ve güç: çayırlar, temel oksitler, karbonatlar ve magnezyum ile etkileşim.
- Silisik asit ve її tuzları. Rozchinne slo.
- Zastosuvannya silikon ve yogo yarısı.
- Sklo.
- Çimento.
günü adlandır
Çoğu zaman doğada silikon, silis benzeri bir görünümde bulunur - silikon dioksit (IV) Si02'ye (dünyanın kızamık kütlesinin yaklaşık %12'si) dayalı bir baz. Silisyum dioksit ile söndürülen ana mineraller ve kayaçlar, zincir (zengin ve kuvars), kuvars ve kuvarsit, çakmaktaşı, polov_spar'dır. Doğada genişlik için silika ve alüminosilikat birbirine katlanır.
Saf silisyumun doğal görünümündeki önemi birer birer not ediliyor.
Otrimannya
Magnezyum ile çıtır beyaz pisku (silikon dioksit) kızartıldığında silikon çıkacaktır:
S ben Ö 2 + 2 M g → 2 M g Ö + Si (\displaystyle ~(\mathsf (SiO_(2)+2Mg\ \rightarrow \ 2MgO+Si)))neye yerleşirsin şekilsiz silikon , kahverengi toz gibi görünebilir.
Sanayide silikon teknik saflığı, şaft tipi cevher-termal fırınlarda SiO2'nin kok ile yaklaşık 1800 ° C sıcaklıkta eritilmesiyle elde edilir. Böyle bir dereceyle çıkarılan silikonun saflığı% 99,9'a ulaşabilir (ana evler kömür, metaldir).
Silisyum temizliğinden evlerden uzaklaşabilirsiniz.
- Laboratuar tuvaletlerinde saflaştırma, magnezyum silisit Mg2Si'nin önden bulundurulması yolu ile gerçekleştirilebilir. Gaz benzeri monosilan SiH4'ü çıkarmak için ek hidroklorik veya oktik asitler için magnezyum silisit verdik. Monosilan, rektifikasyon, sorpsiyon ve diğer yöntemlerle saflaştırılır ve ardından yaklaşık 1000 °C sıcaklıkta silikon ve su üzerine yerleştirilir.
- Silikonun endüstriyel ölçekte saflaştırılması, silikonun ara olmayan bir şekilde klorlanması yolu ile gerçekleştirilir. Bununla depo SiCl4, SiHCl3 ve SiH2Cl2'nin yarım katları çözülür. Їх farklı bir şekilde evi temizleyin (kural olarak damıtma ve orantısızlaştırma yoluyla) ve son aşamada 900 ila 1100 °C sıcaklıkta saf su ekleyin.
- Silikon saflaştırması için daha ucuz, daha temiz ve daha verimli endüstriyel teknolojiler geliştirilmektedir. 2010 için onlardan önce, silikonun vekaleten flor ile (klor yerine) saflaştırılması için teknolojiler getirmek mümkündür; damıtmayı silikon monoksite aktaran teknolojiler; kristaller arası sınırlara odaklanan vitray evlere dayalı teknolojiler.
Nihai silikondaki Vmіst domіshok, kütle başına% 10 -8 -10 -6'ya düşürülebilir. Saf silikonun beslenmesi hakkında daha fazla rapor, Polikristalin silikon makalesinde gözden geçirilmiştir.
Mikola, Mikolayovich Beketov tarafından saf bir parçalanma biçiminde silikon elde etme yöntemi.
Fiziksel güç
Silikon kristal kafes, elmas gibi kübik yüzey merkezlidir, parametre a = 0,54307 nm (en yüksek mengene silikondaki diğer polimorfik modifikasyonları kaldırın), ancak Si-Si atomları arasındaki daha büyük bir bağ yoluyla bir bağ ile bir bağda zv'azku SS silisyumun sertliği elmasınkinden önemli ölçüde daha azdır. Silikon çatırdama, sadece 800°C'de ısıtıldığında plastik konuşma haline gelir. Infrachervonogo viprominyuvannya s dozhini khvili 1.1 mikron için prozory. Burnun yükteki ıslak konsantrasyonu 5.81 · 10 · 15 m-3'tür (300 K sıcaklık için).
elektrofiziksel güç
Tek kristal formdaki temel silikon, dolaylı boşluklu bir iletkendir. Çitle çevrili alanın genişliği oda sıcaklığı depolama 1.12 eV ve T \u003d 0 K - 1.21 eV'de. Normal zihinler için silikondaki ıslak yük taşıyıcıların konsantrasyonu 1.5·10 10 cm-3'e yakın olur.
Kristal silisyumun elektrotrofik gücü üzerinde, büyük bir akış karanlıkta dolaşan evler inşa eder. Derin bir iletkenliğe sahip silikon kristallerini çıkarmak için, bor, alüminyum, galyum ve indiyum gibi grup III elementlerinin atomlarını silikona sokun. Silisyuma elektronik iletkenliği olan silikondan kristalleri çıkarmak için atomları tanıtın elementler V-ї fosfor, miş'yak, surma gibi gruplar.
Elektronik cihazlar silikon bazında monte edildiğinde, yüzey topunun malzemeye (onlarca mikrona kadar) tutturulması önemlidir, böylece kristalin yüzey kalitesi silikonun elektrostatik gücüne eklenebilir ve görünüşe göre, bitmiş aracın gücü üzerinde. Bazı cihazların montajı sırasında, yüzeyin modifikasyonuna uygulanan vicorous eklenir, örneğin, yüzey çeşitli kimyasal maddeler ve її oprominenya ile silikon ile kaplanır.
Kimyasal güç
Karbon atomlarına benzer şekilde, silikon atomları da orbitallerin sp3-hibridizasyonu ile karakterize edilir. Hibridizasyonla bağlantılı olarak, saf kristal silisyum, silisyumun chotivalent olduğu elmas benzeri taneler yapar. Aynı zamanda, silikon sesi de +4 veya -4 oksidasyon durumuna sahip bir chotivalent element olarak kendini gösterir. Zustrichayutsya iki değerlikli yarı silikon, örneğin, silikon oksit (II) - SiO.
Normal zihinler için, silikon kimyasal olarak aktif değildir ve aktif olarak yalnızca uçucu silikon tetraflorür SiF4'ün çözüldüğü gaz benzeri flor ile reaksiyona girer. Silisyumun bu tür "hareketsizliği", ekşi, tekrar tekrar suyun (su buharı) mevcudiyetinde negatif olarak yerleşen nano boyutlu silikon dioksit topunun yüzeyinin pasivasyonundan kaynaklanır.
çözünmüş Si02 dioksit ile asitleştirme, işleme yüzeydeki dioksit topunun hacminde bir artış eşlik eder, oksidasyon işleminin stabilitesi atomik asit difüzyonu ve kriyoprezervasyon dioksit ile sınırlıdır.
400-500 ° C'nin üzerindeki bir sıcaklığa ısıtıldığında, silikon klor, brom ve iyot ile reaksiyona girer - katlanmış bir depoda kolayca uçucu tetrahalidler SiHal 4 ve muhtemelen halojenürlerin benimsenmesiyle.
Ortası olmayan su silikonu ile reaksiyona girmez, ancak su silikonu ile - Si n H 2n + 2 formülüne sahip silanlar - dolaylı bir yola sahiptir. Monosilan SiH 4 (yogo genellikle basitçe silan olarak adlandırılır), metal silisitlerin asitlerle etkileşiminde görülür, örneğin:
C a 2 S ben + 4 H C l → 2 C a C l 2 + S ben H 4 (\displaystyle ~(\mathsf (Ca_(2)Si+4HCl\ \rightarrow \ 2CaCl_(2)+SiH_(4)\ ) yukarı ok)))Bu reaksiyonda eriyen SiH 4 silan, evlerin ve diğer silanların, zokrem, Si 2 H 6 disilan ve Si 3 H 8 trisilanın, bazı mızraklarda silisyum atomları için tekli bağlarla birbirine bağlanmasının (-Si -Si-Si-) intikamını alır. ) .
Silikon nitrojen ve bor ile 1000 °C'ye yakın sıcaklıklarda reaksiyona girerek nitrür Si3N4'ü ve termal ve kimyasal olarak kararlı borit SiB3, SiB6 ve SiB12'yi çözer.
1000 ° C'nin üzerindeki sıcaklıklarda, periyodik tabloya en yakın analog olan silikon - karbon - yüksek sertlik ve düşük kimyasal aktivite ile karakterize edilen silisyum karbür SiC (karborundum) kullanmak mümkündür. Carborundum, aşındırıcı bir malzeme olarak yaygın olarak kullanılmaktadır. Bununla birlikte, bununla birlikte, silikonun erimesi (1415 °C), izostatik preslemenin büyük sinterlenmiş ince taneli grafit parçaları göz önüne alındığında, pratik olarak değişmeyen ve geri kalanıyla karışmayan kömürle üç saat boyunca temas ettirilebilir.
4. grubun alt elementleri (Ge, Sn, Pb) diğer metallerin çoğunda olduğu gibi silikonda kaplanmamıştır. Silikon ve metallerle ısıtıldığında yarım kabukları olan silisitler oluşturulabilir. Silisitler iki alt gruba ayrılabilir: iyonik-kovalent (su birikintisi, su birikintisi metalleri ve magnezyum tipi Ca2Si, Mg2Si ve in silisitleri) ve metal benzeri (geçiş metallerinin silisitleri). Aktif metallerin silisitleri, asitlerin seyreltilmesi altında ortaya konur; Metal benzeri silisitler yüksek bir erime noktasına sahiptir (2000 °C'ye kadar). Metal benzeri silisit depoları en sık kullanılanlardır. Ben Si, Ben 3Si2, Ben 2 Si 3 , Ben 5 Si 3 ben Ben Si 2 . Metal benzeri silisitler kimyasal olarak inerttir, yüksek sıcaklıklarda ekşiliğe karşı dirençlidir.
Silisyumun, ferrosilikon seramiklerin sızdırmazlığı için malzemelerin, contanın ve silikonun erime sıcaklığından önemli ölçüde daha düşük, daha düşük sıcaklıklarda eklenmesine (kaynaşmasına) izin veren ötektik toplamı kapattığını not etmek özellikle önemlidir.
1200 °C'nin üzerindeki sıcaklıklarda silisyuma SiO2 eklendiğinde silikon oksit (II) - SiO çözülür. Bu süreç, kristallerin silikon yöntemlerle üretilmesi ile sürekli olarak desteklenmektedir.
1811'de vizyonların ön saflarında silikon. J.Gay-Lussac ve L.Tenar, silikon florür buharlarını potasyum metali üzerinden geçirirken, proteinler onlar tarafından bir element olarak tanımlanmıyor. 1823'te İsveçli kimyager J. Berzelius potasyum tuzu K2SiF6'nın metal potasyum ile yüksek sıcaklıkta işlenmesi sırasında çıkardığı silikonun bir tanımını vererek. Yeni elemente "silikyum" (Lat. silex - çakmaktaşı) adı verildi. Rus adı "silikon", 1834 yılında Rus kimyager Herman Ivanovich Hess tarafından tanıtıldı. Diğer Yunanca çeviride. krhmnoz- Kut, dağ.
Doğadaki bilgi, otrimannya:
Doğada silikon, farklı bir depoda titreşen dioksit ve silikatlarda bulunur. Doğal silikon dioksit, diğer mineralleri kullanmak isteyen kuvars formunda daha önemlidir - kristobalit, tridimit, balina, cosite. Amorf silis, denizlerin ve okyanusların dibindeki diatom birikintilerinde birikir - bu birikintiler Si02 ile yerleşerek diatomların ve diğer siliyerlerin deposuna girer.
Vilniy silikon, bir kimya deposu için silikon oksit SiO 2 + 2Mg = 2MgO + Si ile temizlenebilen magnezyum gevrek beyaz pisku ile kavurma için kullanılabilir. Sanayide silisyum teknik saflığı, SiO2'nin kok ile ark fırınlarında yaklaşık 1800 °C sıcaklıkta eritilmesiyle elde edilir. Böyle bir rütbe ile elde edilen silikonun saflığı% 99,9'a ulaşabilir (ana evler kömür, metaldir).
Fiziksel güçler:
Amorf silikon, kalınlığı 2.0 g / cm3 daha yoğun olan kahverengi bir toz gibi görünebilir. Kristal silikon - koyu gri, parıldayan kristal konuşma, kristalize ve sert, elmaslarda kristalleşir. Bu tipik bir iletkendir (elektriği iletmek daha iyidir, yalıtkan tip kauçuk daha düşüktür ve bir iletken - orta için daha yüksektir). Silikon çatırdama, sadece 800°C'de ısıtıldığında plastik konuşma haline gelir. Cіkavo, 1.1 mikron uzun bir rüzgarla başlayan infrachervony viprominyuvannya'ya scho silisli prosorium.
Kimyasal güç:
Kimyasal olarak silikon düşük aktif. Oda sıcaklığında sadece gaz benzeri flor ile reaksiyona girer, uçucu silikon tetraflorür SiF 4 bu sıcaklıkta çözünür. 400-500 ° C'lik bir sıcaklığa ısıtıldığında, silikon asit ile çözünmüş dioksit, klor, brom ve iyot ile - çözünmüş kolayca uçucu tetrahalidler SiHal 4 ile reaksiyona girer. 1000 ° C'ye yakın sıcaklıklarda silikon, nitrür Si3N4'ü bor - termal ve kimyasal olarak kararlı borür SiB3, SiB6 ve SiB12 ile çözmek için azotla reaksiyona girer. Sulu silikon ile sorunsuz reaksiyona girmez.
Silisyum ile aşındırma için, en yaygın olarak hidroflorik ve nitrik asitlerin toplamı kullanılır.
Çayırlara ayarlayın.
Silikon, +4 veya -4'lük bir oksidasyon adımı ile karakterize edilir.
En önemli alanlar:
Silikon dioksit, SiO 2- (Silikon anhidrit) ...
...
silisik asitler- zayıf, belirsiz, utvoryuyuyutsya asit eklendiğinde silikatın boyutu jel gibi görünür (jelatin benzeri konuşma). H4Si04 (orto-silikon) ve H2Si03'ün (meta-silikon veya silikon) yalnızca değiştiği ve ısıtıldığında ve kurutulduğunda geri dönülmez bir şekilde Si02'ye dönüştüğü bilinmektedir. Girilecek katı gözenekli ürün - silika jeli yüzeyde açılabilir ve bir gaz adsorbanı, bir kurutma maddesi, bir katalizör ve bir aşınma katalizörü olarak zararlı olabilir.
silikat- iyinin silisik asit tuzları (sodyum ve potasyumun kristal silikatları) suda çözünmez. güç.
şelaleler- karbonhidrat analogları, silani, isteksizce, tek bağa sahip silikonun bazı atomlarında, kuvvet yakscho atom silikon z'єdnаnі podvіyny zv'yazkom. Lances ve kiltsya, karbonhidratlara benzer şekilde kullanılır. Tüm güçler bağımsız olarak kullanılabilir, tekrarlı sumish titreşimleri yapabilir ve su ile kolayca reaksiyona girebilir.
Zastosuvannya:
En önemli silikon miktarı, alüminyum, bakır ve magnezyum uygulamaları için alaşımların seçiminde ve çeliklerin ve ısıtma ekipmanının seçiminde önemli olabilecek ferosilisitlerin seçiminde bilinmektedir. Silikon kristaller zastosovuyut sony piller ve napіvprovіdnikovih ek binalar - transistörler ve diyotlar. Silikon ayrıca, yağ, yağ, plastik ve sentetik kauçuklarla lekelenen organosilikon levhaların veya siloksanların üretimi için sirovina görevi görür. inorganik salyangozlar silikon vikorist, seramik ve çelik teknolojisinde, yalıtkan bir malzeme olarak ve p'ezocrystals olarak kullanılır.
Bazı organizmalar için silikon önemli bir biyojenik elementtir. Yaratıklarda roslin ve iskeletteki destekleyici kulübelerin deposuna girin. Deniz organizmaları - diyatomlar, algler, radyolarya, süngerler - geniş silikon alanlarında yoğunlaşmıştır. Büyük sayılar atkuyruğu ve tahıllar, ilk siyahta - Bambu ve Pirinç benzeri pidrodinlerde, aralarında - pirinç ekiminde silikon ile konsantre olur. Bir kişinin M'yazova dokusu intikam almak için (1-2) %10 -2 silikon, kemik dokusu - 17 %10 -4, kan - 3,9 mg/l. Ancak günümüzde bir insanın vücuduna 1 grama kadar silikon alınabilmektedir.
Antonov S.M., Tomilin K.G.
HF Tyumen Eyalet Üniversitesi, 571 grubu.
